En utilisant une analyse FRET à une seule molécule, une équipe de chercheurs a révélé comment les différentes conformations de la protéine de pointe du coronavirus 2 (SRAS-CoV-2) du syndrome respiratoire aigu sévère sont interconnectées. Déterminer les différentes conformations en temps réel et quelles conformations les anticorps préfèrent peut aider à concevoir des vaccins et des médicaments efficaces. La recherche est publiée sur le serveur de pré-impression bioRxiv*.
Les illustrations du virus SRAS-CoV-2 ressemblent généralement à une boule épineuse. Les pointes qui sortent de la surface du virus sont appelées protéines de pointe (S). Ces protéines de pointe permettent au virus de pénétrer dans une cellule hôte, provoquant une infection.
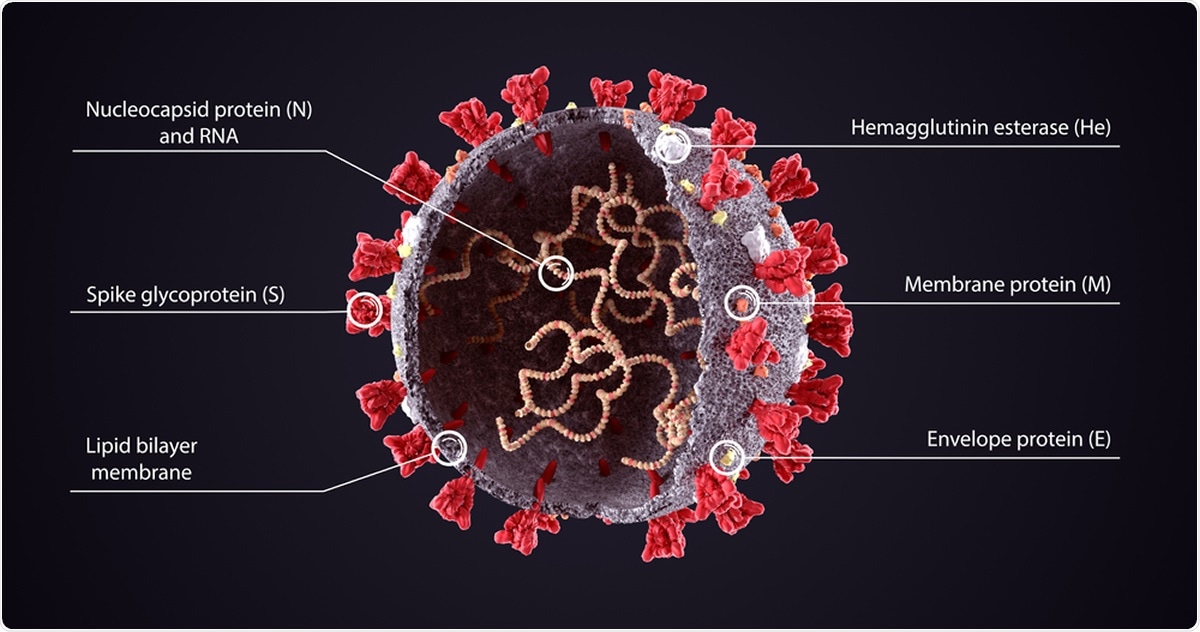
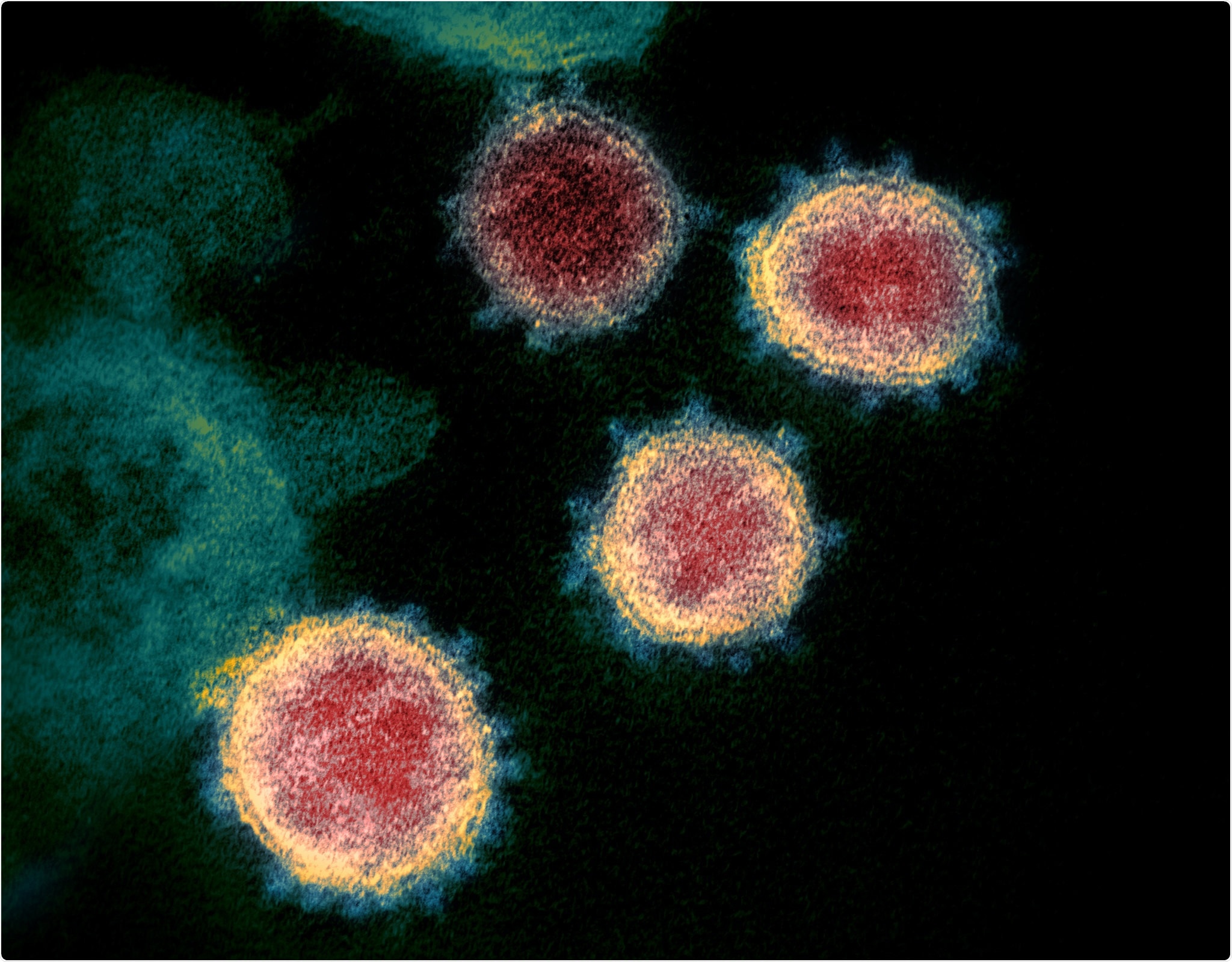
Illustration du SRAS-CoV-2. Crédit d'image: Orpheus FX / Shutterstock
La protéine de pointe a deux parties, une tête (S1), assise sur un corps en forme de bâton (S2). La tête se lie à des récepteurs appropriés sur la cellule hôte en utilisant certaines parties appelées les domaines de liaison aux récepteurs (RBD). Le corps en forme de bâtonnet provoque alors la fusion de l'enveloppe du virus avec la membrane de la cellule hôte. La fusion du virus à la cellule humaine se produit lorsque l'enzyme de conversion de l'angiotensine humaine 2 (hACE2) se lie aux RBD.
Des études ont révélé que la protéine de pointe peut avoir différentes conformations. Dans l'un, dans lequel tous les RBD sont orientés vers le bas de sorte que ces récepteurs sont inaccessibles pour la liaison. Une seconde, où un ou deux RBD sont orientés vers le haut, et une troisième orientation avec tous les RBD sont orientés vers le haut, où tous les récepteurs sont accessibles. Cependant, comment ces différentes conformations sont interconnectées et comment elles se comportent est encore inconnue.
Quatre conformations différentes de la protéine de pointe
Pour comprendre les différentes conformations en temps réel, une équipe de chercheurs a utilisé le transfert d'énergie de résonance de Förster à molécule unique (FRET). Dans FRET, l'énergie est transférée entre deux molécules sensibles à la lumière. Puisque l'efficacité du transfert d'énergie est liée à la distance entre les deux molécules, FRET est utilisé pour comprendre la distance entre deux parties d'une molécule à laquelle les molécules sensibles à la lumière sont attachées.
En utilisant les structures disponibles de la protéine de pointe, les chercheurs ont marqué des sites avec des fluorophores qui peuvent être utilisés pour détecter les changements de distance entre les fluorophores avec des changements dans les conformations. L'équipe a excité les protéines marquées par fluorescence à l'aide d'un laser vert et a enregistré l'émission.
Les chercheurs ont trouvé des rendements FRET faibles (~ 0,1), intermédiaires (~ 0,3 et ~ 0,5) et élevés (~ 0,8). Ils disent que cela correspond à au moins quatre conformations différentes de la protéine de pointe. La conformation à efficacité FRET intermédiaire était la plus abondante, basée sur le comptage de plusieurs centaines de traces FRET.
Les auteurs disent que la conformation intermédiaire correspond à tous les RBD pointant vers le bas, vers la surface du virus. Ils ont constaté qu'un pont disulfure entre deux acides aminés stabilise la protéine de pointe, qui, sur la base d'études précédentes, correspond à l'orientation vers le bas.
Lorsqu'ils ont utilisé le récepteur hACE2 qui se lie aux RBD, ils ont trouvé que l'état de FRET bas était plus abondant, suggérant que tous les RBD étaient orientés vers le haut, ou loin de la surface du virus, lorsqu'ils étaient liés aux récepteurs.
La protéine de pointe était en équilibre entre les différentes conformations à pH physiologique et à température ambiante. Lorsque les conformations ont changé, il y avait un ordre spécifique dans lequel elles ont transité; d'abord de l'état de rendement faible à intermédiaire, puis de l'état de rendement intermédiaire à l'état de rendement élevé.
Ainsi, il existe une séquence spécifique d'activation des transitions structurelles dans la protéine de pointe SARS-CoV-2. La conformation RBD-down change en la conformation RBD-up, qui est activée par le récepteur, via au moins une conformation intermédiaire.
Les anticorps ont au moins deux mécanismes de neutralisation
Ensuite, l'équipe a analysé ce qui arrive aux conformations lorsque les anticorps se lient. En utilisant le plasma de deux patients en convalescence, où les anticorps dans le plasma se lient à la protéine de pointe, ils ont trouvé que la protéine de pointe était dans la conformation RBD-up pour les anticorps d'un patient. Cela était similaire à l'orientation utilisant le récepteur hACE2.
Les anticorps de l'autre patient ont stabilisé la conformation RBD-down. Bien que les anticorps aient contrarié la liaison du récepteur hACE2, «mais la compétition RBD n'a pas affecté sa reconnaissance de S, ce qui suggère que son activité de neutralisation ne repose pas uniquement sur le blocage de l'interface du récepteur», écrivent les auteurs.
Les résultats suggèrent que le virus SARS-CoV-2 peut être neutralisé de différentes manières. Premièrement, par des anticorps imitant le récepteur hACE2 et en compétition avec lui pour se lier à la protéine de pointe; et deux, en stabilisant la protéine dans la conformation RBD-down, empêchant la liaison à la cellule hôte.
Par conséquent, les stratégies de conception de vaccins ou de médicaments efficaces peuvent utiliser différentes approches pour se lier à la protéine de pointe du SRAS-CoV-2.
*Avis important
bioRxiv publie des rapports scientifiques préliminaires qui ne sont pas examinés par des pairs et, par conséquent, ne doivent pas être considérés comme concluants, orienter la pratique clinique / les comportements liés à la santé, ou traités comme des informations établies.

_987e327fa8274297bf6da4dd3c95ee69-620x480.jpg)