Une équipe de scientifiques français a récemment mené une étude pour évaluer la sensibilité du variant B.1.617 du coronavirus 2 du syndrome respiratoire aigu sévère (SRAS-CoV-2) à la neutralisation par anticorps. Les résultats révèlent que, comparé aux autres variants circulants, le variant B.1.617 est résistant aux anticorps monoclonaux thérapeutiques et aux anticorps naturels induits par une infection ou un vaccin. L’étude est actuellement disponible sur le bioRxiv* serveur de pré-impression.
Sommaire
Arrière-plan
Avec la progression de la pandémie de maladie à coronavirus 2019 (COVID-19), plusieurs nouvelles variantes du SRAS-CoV-2 sont apparues dans le monde. En raison de l’acquisition de multiples mutations de pointe, nombre de ces variantes ont acquis des avantages évolutifs, notamment une infectivité et une virulence accrues et la capacité d’échapper aux réponses immunitaires de l’hôte. En octobre 2020, une nouvelle lignée SRAS-CoV-2 appelée B.1.617 a émergé en Inde, provoquant une augmentation exponentielle des cas de COVID-19 à travers le pays. La lignée est divisée en trois sous-groupes: B.1.617.1, B.1.617.2 et B.1.617.3; dont la variante B.1.617.2 a été désignée comme variante préoccupante (COV) en raison d’une infectivité considérablement accrue. Cependant, on ne dispose pas de suffisamment d’informations sur la sensibilité de cette lignée à l’hôte de l’immunité humorale.
Dans la présente étude, les scientifiques ont étudié la sensibilité du variant B.1.617.2 aux anticorps monoclonaux thérapeutiques et aux anticorps dérivés d’individus récupérés ou vaccinés contre le COVID-19.
Étudier le design
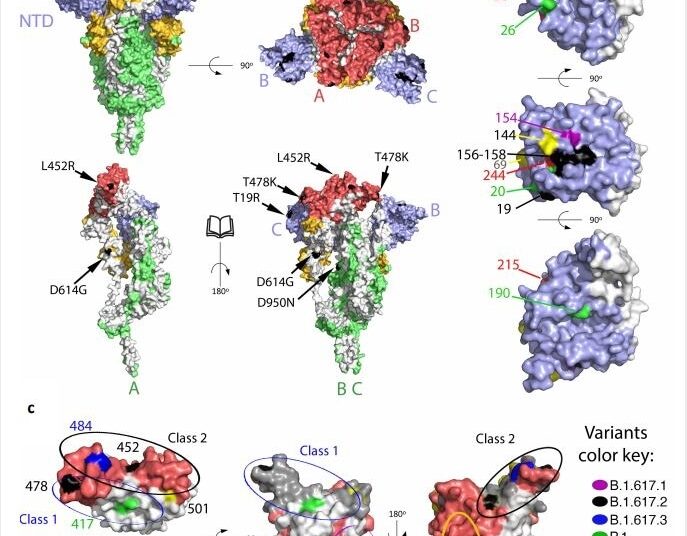
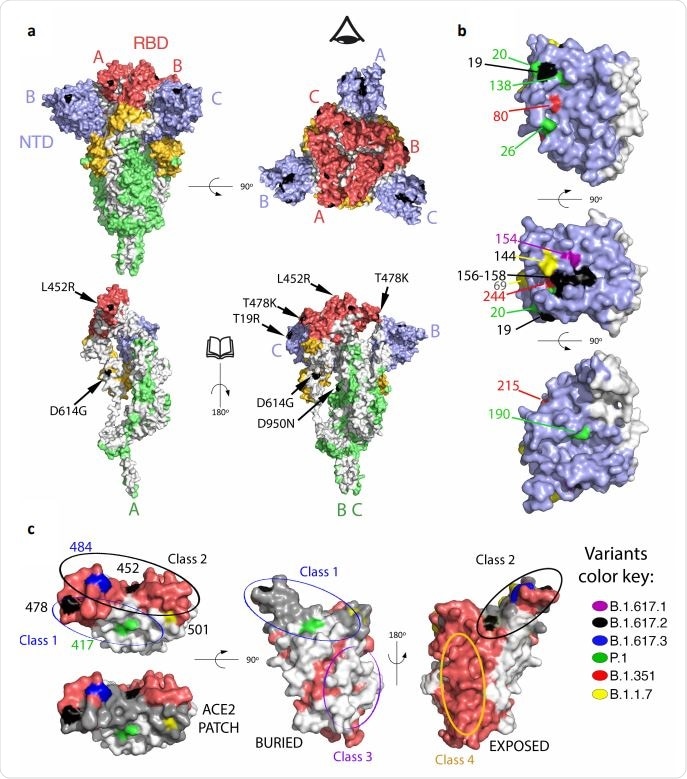
Dans l’étude, le variant B.1.617.2 a été isolé à partir de l’échantillon sur écouvillon nasopharyngé d’un individu. Comparé au variant D614G de SARS-CoV-2, le variant B.1.617.2 contient neuf mutations de pointe, dont cinq mutations dans le domaine N-terminal (NTD), 2 mutations dans le domaine de liaison au récepteur (RBD), 1 mutation dans le site de clivage de la furine et une mutation dans la sous-unité de pointe S2.
Pour examiner le potentiel de fuite immunitaire du variant, quatre anticorps anti-RBD cliniquement approuvés ainsi que quatre autres anticorps anti-RBD et quatre anticorps anti-NTD ont été inclus.
Pour l’isolement des anticorps, des échantillons de sérum ont été prélevés sur 56 individus récupérés par COVID-19 et 28 individus vaccinés. Parmi les individus vaccinés, 16 ont reçu le vaccin Pfizer à base d’ARNm et 12 ont reçu le vaccin AstraZeneca à base d’adénovirus.
Caractérisation génétique du variant B.1.617.2
Les mutations de pointe identifiées dans la variante B.1.617.2 ont montré un schéma de distribution similaire à celui des autres COV. Outre la mutation D614G, la mutation D950N a été identifiée dans l’interface trimère. La majorité des mutations NTD étaient présentes dans le «supersite», qui est la cible principale des puissants anticorps neutralisants anti-NTD. De même, toutes les mutations RBD ont été identifiées dans la périphérie de la surface de liaison de l’enzyme de conversion de l’angiotensine 2 (ACE2), indiquant que le variant B.1.617.2 acquiert ces mutations pour éviter la liaison de l’anticorps sans entraver la liaison de l’ACE2.
Neutralisation médiée par un anticorps monoclonal du variant B.1.617.2
Tous les anticorps thérapeutiques testés (Bamlanivimab, Etesevimab, Casirivimab et Imdevimab) ont montré une puissance élevée dans la neutralisation du variant D614G. À l’exception de l’Etesevimab, les trois autres anticorps ont également neutralisé activement le variant B.1.1.7.
En ce qui concerne le variant B.1.617.2, tous les anticorps à l’exception du Bamlanivimab ont conservé leur pouvoir actif de neutralisation virale. L’acquisition de la mutation L452R pourrait être la mutation d’échappement pour Bamlanivimab.
Sur quatre autres anticorps anti-RBD, trois ont neutralisé efficacement le variant B.1.617.2. En revanche, trois anticorps anti-NTD sur quatre n’ont pas réussi à neutraliser le variant B.1.617.2, le quatrième présentant une efficacité neutralisante modeste.
L’analyse cytométrique en flux pour déterminer l’interaction anticorps-variant a révélé que le variant B.1.617.2 a développé une résistance à la neutralisation médiée par anticorps principalement en empêchant la liaison anticorps-épitope.
Neutralisation par sérum de convalescence du variant B.1.617.2
Les échantillons de sérum obtenus à partir d’individus récupérés de COVID-19 après six mois d’apparition des symptômes ont été testés contre les variants B.1.617.2, D614G, B.1.1.7 et B.1.351. Par rapport aux variantes D614G et B.1.1.7, la variante B.1.617.2 a montré une sensibilité 4 à 6 fois inférieure à la neutralisation par des sérums de convalescence.
De même, des échantillons de sérum prélevés sur 48 travailleurs de la santé en convalescence après 12 mois d’apparition des symptômes ont montré une puissance six fois plus faible pour neutraliser la variante B.1.617.2 par rapport à la variante B.1.1.7. Parmi les travailleurs de la santé, 13 ont reçu le 1st dose du vaccin AstraZeneca, Pfizer ou Moderna COVID-19. Les sérums obtenus des agents de santé vaccinés ont montré une augmentation de 130 fois des taux d’anticorps neutralisants contre les variants B.1.617.2 et B.1.1.7. Ces résultats révèlent que le variant B.1.617.2 est comparativement moins sensible à la neutralisation par des sérums de convalescence obtenus 1 an après l’infection.
Neutralisation médiée par la vaccination du variant B.1.617.2
Les sérums obtenus à partir d’individus complètement immunisés avec le vaccin Pfizer COVID-19 ont montré une puissance 3 fois et 16 fois plus faible pour neutraliser les variants B.1.617.2 et B.1.351, respectivement, par rapport au variant B.1.1.7 . En revanche, les sérums obtenus à partir d’individus immunisés avec une dose unique du vaccin AstraZeneca COVID-19 ont montré une puissance significativement plus faible pour neutraliser le variant B.1.617.2.
Importance de l’étude
Les résultats de l’étude révèlent que le variant B.1.617.2 récemment apparu du SRAS-CoV-2 est partiellement résistant à la neutralisation par des anticorps monoclonaux anti-RBD et anti-NTD et des anticorps polyclonaux induits par une infection ou une vaccination naturelle du SRAS-CoV-2.
*Avis important
bioRxiv publie des rapports scientifiques préliminaires qui ne sont pas évalués par des pairs et, par conséquent, ne doivent pas être considérés comme concluants, orienter la pratique clinique / les comportements liés à la santé ou être traités comme des informations établies.