La maladie à coronavirus 2019 (COVID-19) est une maladie respiratoire causée par le coronavirus-2 du syndrome respiratoire aigu sévère (SARS-CoV-2). Les symptômes du COVID-19 comprennent une fièvre légère à sévère, une toux et des maux de tête, bien que certaines personnes puissent avoir des réponses immunitaires massives, une insuffisance respiratoire, une hospitalisation et même la mort. Les facteurs de risque du COVID-19 comprennent l'âge avancé, le sexe masculin, les maladies cardiovasculaires et rénales, l'obésité et la maladie pulmonaire obstructive chronique, entre autres.
Cela fait presque un an depuis l'entrée zoonotique du SRAS-CoV-2 dans la population humaine. À ce jour, il a infecté plus de 50 millions de personnes, causant plus de 1,25 million de décès dans le monde. La pandémie qui en a résulté a également provoqué des perturbations économiques et sociétales généralisées, faisant de l'invention d'un vaccin une question de toute urgence. Les principaux candidats vaccins contre le SRAS-CoV-2 utilisent des vecteurs viraux pour délivrer la protéine de pointe virale aux cellules cibles. Ces vecteurs sont codés par des ARNm.
Récemment, des chercheurs de la Johns Hopkins University School of Medicine, Baltimore, MD, États-Unis, et de Capricor Therapeutics, Inc., Beverly Hills, Californie, États-Unis, ont décrit une nouvelle approche du développement d'un vaccin contre le SRAS-CoV-2 utilisant des exosomes pour délivrer des ARNm qui codent pour les antigènes de plusieurs protéines structurales du virus. Leur étude a été démontrée sur le serveur de pré-impression bioRxiv *.
« Dans le présent rapport, nous avons établi que les formulations d'exosomes purifiés, d'ARNm synthétisés in vitro et de lipides polycationiques peuvent médier le transport de l'ARNm dans les cellules humaines et l'expression fonctionnelle des produits protéiques codés par l'ARNm. »
Sommaire
Livraison médiée par les exosomes d'ARNm codant pour les protéines structurales du SRAS-CoV-2
Les chercheurs ont purifié les exosomes et les ont chargés avec les ARNm conçus pour exprimer une protéine de fusion artificielle – LSNME – qui contient des parties des protéines virales de pointe, de membrane, de nucléocapside et d'enveloppe également une forme fonctionnelle de la protéine de pointe.
Le vaccin combiné résultant – LSNME / SW1 – a été injecté à des souris C57BL / 6J âgées de 13 semaines, et les réponses immunitaires humorales et cellulaires à la nucléocapside et aux protéines de pointe du SRAS-CoV-2 ont été évaluées. Des analyses hématologiques et histologiques ont également été effectuées pour rechercher d'éventuels effets indésirables chez les animaux vaccinés.
Les souris immunisées présentent des réponses des lymphocytes T CD4 + et CD8 + aux protéines SARS-CoV-2
Les souris immunisées ont développé des réponses des lymphocytes T CD4 + et CD8 + à la fois à la protéine de nucléocapside et à la protéine de pointe du virus SARS-CoV-2. Ces réponses ont été détectées près de deux mois après la vaccination, comme prévu dans le cas d'une réponse durable à la vaccination. Les chercheurs ont découvert que la réponse des lymphocytes T CD4 + à la protéine de pointe était associée à une expression accrue de l'interféron-gamma. Cela indique une réponse Th1 et une moindre induction de l'interleukine 4, une cytokine associée à Th2.
Les souris vaccinées n'ont montré aucun signe de croissance altérée, d'hypersensibilité au site d'injection, de modification du profil des globules blancs ou de modification de la morphologie des organes. Conformément à ces résultats, l'équipe a également détecté des anticorps anti-nucléocapside et anti-pic modérés dans le plasma des souris vaccinées.
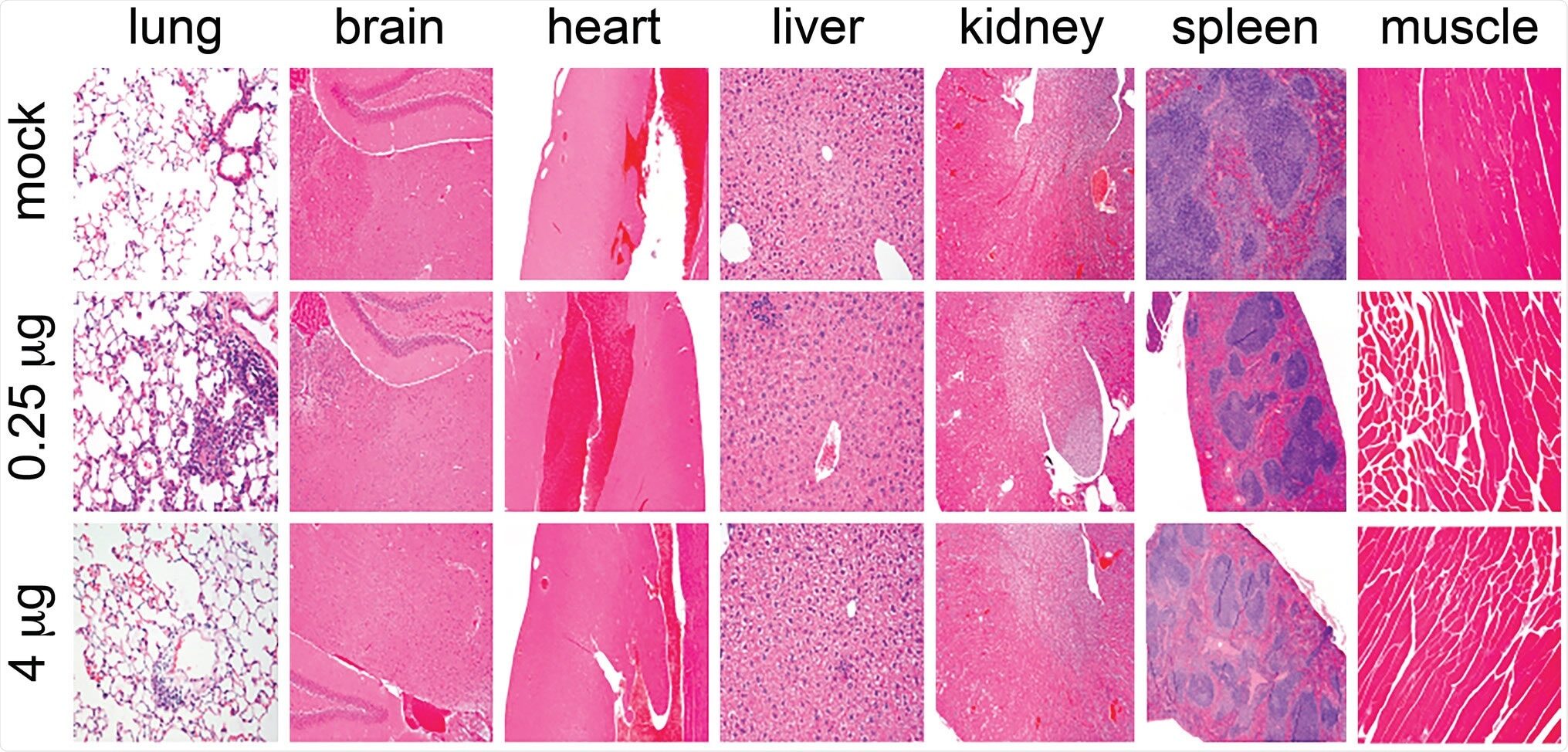
Absence de pathologie tissulaire lors de la vaccination LSNME / SW1. Micrographies représentatives de l'analyse histologique (coloration à l'hématoxyline et à l'éosine) des poumons, du cerveau, du cœur, du foie, des reins, de la rate et des muscles (côté de l'injection) d'animaux provenant de souris témoins (rangée supérieure), de souris (rangée médiane) immunisées avec le dose du vaccin LSNME / SW1 et souris (rangée inférieure) immunisées avec la dose la plus élevée du vaccin LSNME / SW1.
Les résultats valident l'utilisation d'exosomes pour délivrer des ARNm dans les cellules cibles
Dans cette étude, les chercheurs ont établi que les exosomes purifiés peuvent transporter avec succès l'ARNm dans les cellules humaines pour l'expression fonctionnelle des protéines codées par l'ARNm. Ils l'ont d'abord établi pour une protéine fluorescente bioluminescente appelée Antares2 qui a agi comme une protéine rapporteur pour déterminer l'impact de différentes formulations d'exosomes-ARNm sur la délivrance d'ARNm médiée par les exosomes.
Dans l'ensemble, les résultats de l'étude valident l'utilisation d'exosomes dans la délivrance d'ARNm fonctionnels dans des cellules cibles in vitro et in vivo. Plus spécifiquement, les résultats prouvent que le vaccin LSNME / SW1 peut induire une large immunité contre divers types de protéines SARS-CoV-2.
Selon les auteurs, le développement réussi du vaccin LSNME / SW1 à l'avenir dépendra d'études de suivi sur des modèles animaux plus grands à des doses comparables à des vaccins à ARNm similaires qui démontrent avec succès une combinaison de réactions immunitaires sûres et équilibrées ainsi qu'une protection. contre le virus SARS-CoV-2.
« L'utilisation réussie d'exosomes pour délivrer l'ARNm d'Antares2 ouvre la porte à des études de suivi visant à optimiser les conditions de formulation de l'exosome-ARN, ainsi qu'à caractériser la dépendance temporelle de l'expression d'Antares2, la biodistribution de l'expression d'ARN médiée par les exosomes, l'injection effets de site et tissu médié par les exosomes. «
*Avis important
bioRxiv publie des rapports scientifiques préliminaires qui ne sont pas évalués par des pairs et, par conséquent, ne doivent pas être considérés comme concluants, guider la pratique clinique / les comportements liés à la santé, ou traités comme des informations établies.