Dans une récente étude publiée dans la revue PLoS ONEdes chercheurs espagnols ont effectué une revue systématique de la toxine pneumolysine (PLY) en tant que cible moléculaire pour développer de nouvelles thérapies contre Streptococcus pneumoniae.
Pneumolysine comme cible pour de nouvelles thérapies contre les infections à pneumocoque : une revue systématique. Crédit d’image : Kateryna Kon/Shutterstock
Arrière-plan
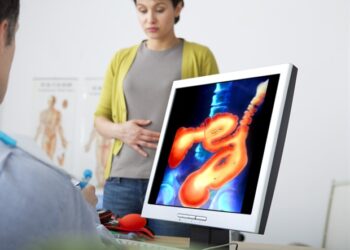
Streptococcus pneumoniae est le principal organisme responsable de la pneumonie communautaire (PAC) chez les enfants et les adultes et provoque également la septicémie, la méningite, l’otite moyenne et la sinusite, malgré la disponibilité des vaccins antipneumococciques. Le PLY est un facteur de virulence clé produit par les organismes pneumococciques et se lie au cholestérol parmi les cellules eucaryotes, et forme des pores entraînant la destruction cellulaire en activant les voies d’apoptose, de pyroptose et de nécroptose, libérant des exosomes et des microvésicules dérivés de la membrane.
Les pores PLY provoquent un afflux substantiel de Ca2+ mitochondrial, déclenchant des changements dans la morphologie mitochondriale et la libération d’acide désoxyribonucléique mitochondrial (ADNmt) via des microvésicules. Au cours de l’inflammation, la toxine active plusieurs voies telles que la protéine kinase activée par les mitogènes (MAPK), le facteur nucléaire kappa-B (NF-κB) et les inflammasomes contenant le domaine 3 de la pyrine du récepteur de type NOD (NLRP3). expression de chimiokines et de cytokines, y compris les interleukines (IL)-1,6,8 et le facteur de nécrose tumorale (TNF). L’émergence de sérotypes vaccinaux non pneumococciques après l’introduction du PCV, associée à la résistance aux antimicrobiens, justifie le développement d’options thérapeutiques plus efficaces pour Streptococcus pneumoniae infections.
À propos de l’étude
Dans la présente étude, les chercheurs ont étudié des molécules ayant une activité inhibitrice directe ou indirecte du PLY et ont exploré les mécanismes d’inhibition du PLY
Des bases de données telles que Scopus, MEDLINE et Web of Science ont été consultées pour trouver des dossiers évaluant PLY en tant que cible moléculaire pour le développement d’agents antipneumococciques, publiés entre le 1er janvier 2000 et le 25 novembre 2021. De plus, les références aux articles inclus ont été examinées. Deux chercheurs indépendants ont examiné tous les dossiers et les désaccords ont été résolus par un autre chercheur. L’équipe a exclu les documents publiés dans des langues autres que l’anglais, y compris les rapports de cas, les brevets, les chapitres de livres, les critiques et les notes.
De plus, les études présentant les toxines PLY comme vaccins et celles élucidant la pathogenèse de l’infection pneumococcique ont été exclues. La qualité des études incluses et les risques de biais ont été déterminés à l’aide des outils de l’Office of Health Assessment & Translation (OHAT). Les données extraites des études incluses comprenaient les auteurs de l’étude, le type de publication, le résumé, le titre, les titres de la source de l’article, l’identificateur d’objet numérique (DOI), la date de publication, les tests effectués sur des animaux de laboratoire et des lignées cellulaires, le dosage testé des molécules, le numéro du Chemical Abstracts Service (CAS), la voie de livraison, le type d’infection et la cause S. pneumoniae souche. De plus, les réseaux de connaissance des molécules anti-PLY ont été évalués.
Résultats
Initialement, 366 enregistrements pertinents ont été obtenus, dont 203, 161 et deux ont été extraits du Web of Science, MEDLINE et Scopus, respectivement. Après suppression des doublons, les titres et les résumés de 192 enregistrements ont été examinés et, après application des critères d’éligibilité, seuls 41 enregistrements évaluant l’activité inhibitrice de PLY de diverses molécules ont été pris en compte pour l’analyse finale. Les molécules peuvent être classées en trois groupes comme suit : (i) les molécules exerçant des effets directs en bloquant ou en se liant avec le PLY, (ii) les molécules à effets indirects en prévenant ses effets délétères sur les cellules de l’hôte, et (iii) les molécules aux propriétés inconnues. mécanismes d’action.
Plusieurs molécules ont été considérées comme des bloqueurs de toxines ; cependant, seuls quelques-uns d’entre eux, notamment les peptides, les antibiotiques, les statines et les stérols, ont le potentiel d’être mis en œuvre pour une utilisation clinique. En revanche, les études démontrant l’efficacité dans les études animales avec une fiabilité adéquate étaient limitées pour d’autres molécules biologiques. La majorité des études avaient un bon niveau de confiance et le risque global de biais dans les études incluses était faible ou probablement faible, mais l’hétérogénéité était élevée.
Les types de molécules anti-PLY comprenaient (i) des composés d’origine végétale (tanins, polyphénols, quinones, flavonoïdes, terpénoïdes et phénéthylamines); (ii) les stérols (β-sitostérol et cholestérol) ; (iii) statines (pravastatine et simvastatine), acides gras oméga-3 [such as docosahexaenoic acid (DHA)]; (iv) purine-6-ones (PDP); (v) thioéthers (montelukast et CysLT1); (vi) antibiotiques (clarithromycine et ceftriaxone); (vii) peptides (TIP et DM3); (viii) des cations (Mg2+Zn2+et Ca2+); et (viii) des anticorps.
Les inhibiteurs PLY directs de l’oligomérisation PLY comprennent l’acacétine, la morine, l’apigénine, le gallate d’épigallocatéchine, la shikonine, la juglone, la quercétine, l’hédéragénine et la dryocrassin ABBA. L’amentoflavone interagit avec PLY au niveau des sites Arg359, Ser254 et Glu277 pour affaiblir l’oligomérisation de PLY, et le verbascoside inhibe l’oligomérisation de PLY en se liant à la fente entre les troisième et quatrième domaines PLY. D’autres molécules inhibitrices directes sont le chlorhydrate d’éphédrine, la bétuline, l’acide oléanolique, le β-sitostérol, l’acide docosahexaénoïque, le peptide DM3, les peptides récepteurs du mannose (MRC-1) et les anticorps anti-PLY.
Les inhibiteurs indirects de PLY comprennent la simvastatine, la 9-(6-phényl-2-oxohex-3-yl)-2-(3,4-diméthoxybenzyl)-purine-6-one, le montélukast, la protéine intrinsèque tonoplaste dérivée du TNF (peptide TIP) , peptide JI-34 agoniste du GHRH, vasculotide, zVAD-fmk, Z-VAL-ALA-OH et Ca2+. Les inhibiteurs de PLY aux mécanismes inconnus comprennent l’aloès-émodine, la clarithromycine, la ceftriaxone, le Mg2+et Zn2+. Les mécanismes d’inhibition indirecte du PLY comprennent la réduction de la teneur en cholestérol et l’inhibition du récepteur du facteur d’activation plaquettaire (PAFr), de la phosphodiestérase 2 (PDE2), du récepteur 1 du cystéinyl leucotriène (CysLT1), du peptide TIP, de la protéine kinase C-alpha et de l’arginase. D’autres mécanismes comprennent la restauration de l’absorption de sodium et l’atténuation de la phosphorylation de la chaîne légère de la myosine (MLC) et des délétions du gène codant pour PLY.
Dans l’ensemble, les résultats de l’étude ont montré que plusieurs molécules anti-PLY réduisaient l’inflammation associée à l’infection pneumococcique, dont certaines sont déjà utilisées à d’autres fins et peuvent donc être considérées comme sûres pour une utilisation contre le pneumocoque. Les patients peuvent bénéficier d’une deuxième ligne de traitement dans les premiers stades de l’infection, prévenant les infections invasives à pneumocoques de type et le syndrome de détresse respiratoire aiguë (SDRA).

























Une étude de Penn State examine comment les télomères d'une personne sont affectés par la restriction calorique