Le coronavirus 2 du syndrome respiratoire aigu sévère (SRAS-CoV-2), identifié comme l’agent causal de la pandémie de COVID-19 (maladie à coronavirus 2019), a été détecté pour la première fois à Wuhan, en Chine, fin décembre 2019. Cependant, aucun médicament ou stratégie de traitement efficace ont été développés depuis lors pour lutter contre les manifestations complexes de la maladie qui affligent les individus de tous âges, conditions de santé et ethnies.
Alors que les vaccins contre le SRAS-CoV-2, développés à un rythme sans précédent, sont administrés pour lutter contre le virus, il existe un besoin urgent de thérapies contre le SRAS-CoV-2 – en particulier avec les menaces émergentes de variantes qui peuvent échapper aux vaccins.
Dans un effort pour accélérer la recherche sur l’identification des médicaments antiviraux pour l’infection par le SRAS-CoV-2, des chercheurs des États-Unis et de la Suisse ont effectué un dépistage approfondi des médicaments pour l’activité antivirale en utilisant une infection virale vivante dans les cellules respiratoires humaines. En conséquence, ils ont identifié un ensemble de candidats-médicaments potentiels qui pourraient potentiellement être testés dans des essais cliniques.
Ils ont observé que la combinaison d’inhibiteurs de la biosynthèse de la pyrimidine avec des analogues de nucléosides antiviraux inhibait de manière synergique l’infection par le SRAS-CoV-2 in vitro et in vivo. Une version pré-imprimée du document de recherche est disponible sur le site medRxiv* serveur pendant que l’article est soumis à une évaluation par les pairs.

«De vastes efforts sont en cours pour identifier les voies hôtes essentielles pouvant être médicamentées et pour réutiliser les thérapies contre ces cibles hôtes.»
Les virus dépendent de la biogenèse des nucléosides de l’hôte pour la réplication virale car ils nécessitent des niveaux élevés de nucléosides triphosphates (NTP) pour leur croissance.
Les virus à ARN, tels que les coronavirus, se répliquent en utilisant une ARN polymérase dépendante de l’ARN (RdRp) codée de manière virale ; à l’intérieur de l’hôte lorsque des analogues nucléosidiques sont mal incorporés au cours du processus, cela peut entraîner une terminaison de chaîne ou une mutagenèse, inhibant finalement la réplication virale. Cela offre une opportunité de tuer le virus en utilisant des analogues et des inhibiteurs appropriés.
Les analogues nucléosidiques sont une classe courante de médicaments qui sont des analogues synthétiques imitant leurs homologues physiologiques. Le remdesivir (approuvé par la FDA pour une utilisation dans le COVID-19) et le Molnupirivir (en essai clinique) sont mal incorporés par le RdRp viral, ce qui entraîne respectivement une terminaison de chaîne retardée et une mutagenèse virale accrue ; réalisant ainsi l’activité antivirale.
Il existe des voies d’entrée distinctes et spécifiques au type cellulaire pour l’entrée et d’autres étapes du cycle de vie viral. Étant donné que les chercheurs de cette étude recherchaient des antiviraux qui seraient actifs dans les voies respiratoires, ils ont utilisé la lignée cellulaire respiratoire humaine Calu-3 pour identifier les antiviraux potentiels.
En utilisant des bibliothèques de petites molécules contenant des médicaments approuvés, des médicaments en essais cliniques et des médicaments avec des cibles connues, les chercheurs ont sélectionné des candidats pour découvrir à la fois des antiviraux à action directe et dirigés par l’hôte. Dans l’étude, ils ont utilisé un virus de type sauvage et un test cellulaire à haute teneur dans les cellules respiratoires et optimisé un test basé sur la microscopie pour obtenir des paramètres de dépistage robustes (Z’> 0,5) en utilisant un véhicule (DMSO) et du Remdesivir (10uM ) comme témoins sur chaque plaque.
18 000 médicaments
Les chercheurs ont passé au crible ~ 18 000 médicaments de trois bibliothèques de réaffectation : une bibliothèque interne PENN de ~ 3 500 médicaments, ~ 3 400 médicaments de la collection de réaffectation du NCATS (National Center for Advancing Translational Sciences) choisie pour éviter tout chevauchement avec la bibliothèque PENN, et le ReFrame collection d’environ 11 300 médicaments dont la plupart ont été testés chez l’homme.
« Au total, nous avons criblé une grande partie des médicaments qui peuvent potentiellement être rapidement réutilisés dans les cellules respiratoires avec un virus vivant complétant les efforts de dépistage précédents. »
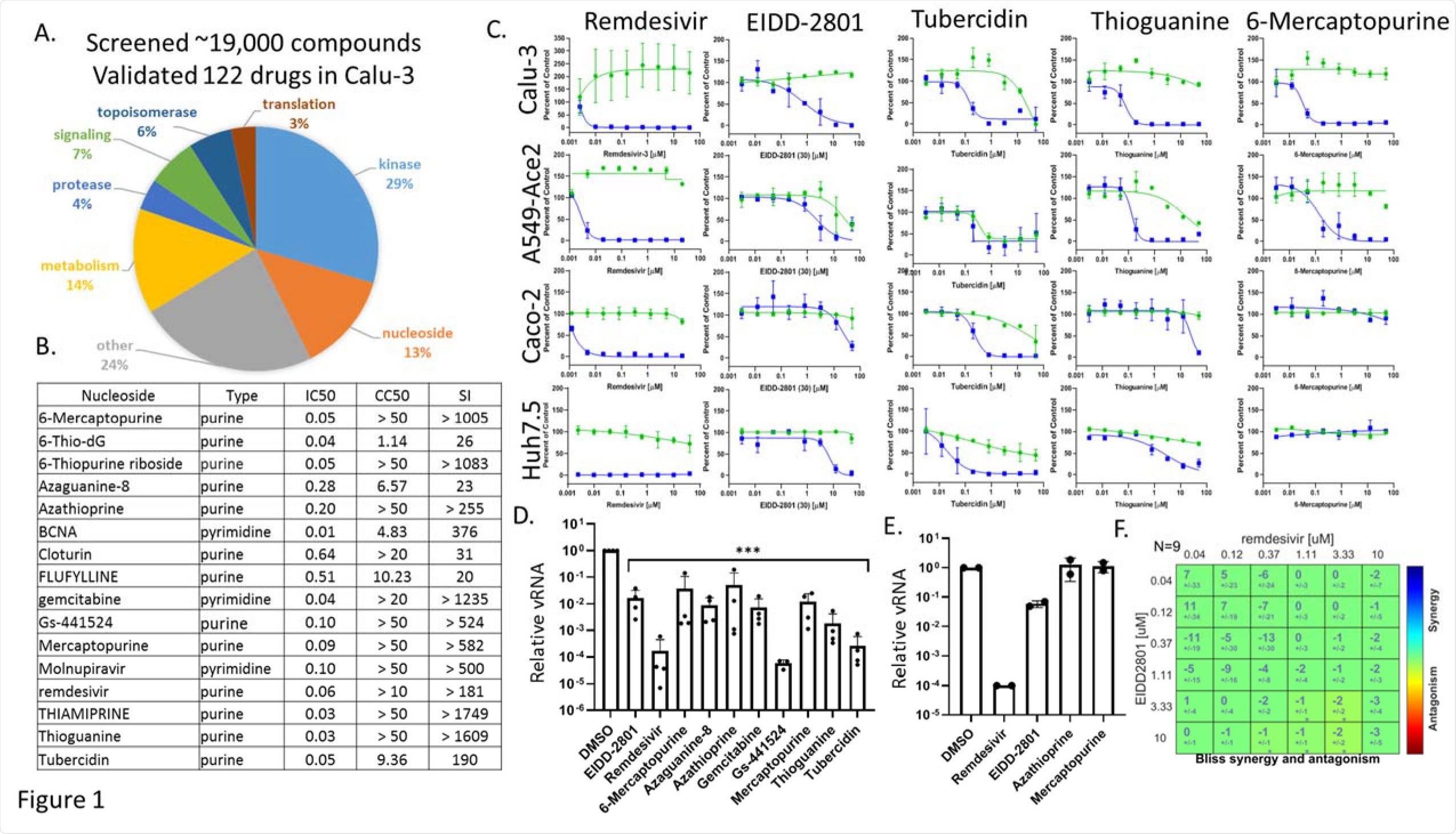
Les nucléosides antiviraux sont très actifs dans les cellules respiratoires et présentent une activité spécifique au type cellulaire. A. Diagramme circulaire des antiviraux validés dans les cellules Calu-3 avec un indice sélectif (EC50/CC50)>3. Sur environ 19 000 composés, 122 présentent une activité. B. 16 analogues nucléosidiques validés dans des cellules Calu-3 avec le type nucléosidique répertorié avec les EC50, CC50 et SI.C. Des cellules Calu-3 A549-ACE2 Caco-2 Huh7.5 ont été traitées avec les nucléosides indiqués en réponse à la dose montrant une infection (bleu) et une toxicité (vert). D. Cellules Calu-3 prétraitées avec le véhicule ou 10 uM des médicaments indiqués et infectées par le SRAS-CoV-2 pendant 48 h et analyse RT-qPCR de l’infection virale avec une moyenne ± SE montrée pour une réduction par rapport au contrôle du véhicule (n≥3). (p < 0,001, ANOVA) E. Analyse RT-qPCR de l'infection virale montrée pour les médicaments indiqués dans les cultures d'interface air-liquide nasale ; Remdesivir (10 uM), EIDD-2801 (10 uM); Azathioprine (30 uM); Mercaptopurine (30 uM). (n=2).G. Analyse BLISS de la combinaison 2x2 de Remdesivir et Molnupiravir dans des cellules Calu-3 montrant une additivité.
Analogues nucléosidiques
Avec le Remdesivir et le Molnupirivir, les chercheurs ont identifié d’autres analogues nucléosidiques dotés de propriétés antivirales contre le SRAS-CoV-2. Les chercheurs ont également déterminé l’étendue de l’activité antivirale en testant ces analogues de nucléosides dans un panel de lignées cellulaires infectées – qui sont permissives à l’infection par le SRAS-CoV-2, comme l’ACE2 respiratoire humain exprimant l’A549, l’épithélial intestinal humain Cellules Caco-2, l’hépatocyte humain Huh7.5 et les cellules Vero de singe vert d’Afrique. En outre, ils ont démontré que le Remdesivir et le Molnupirivir présentaient une activité sur divers types de cellules.
Les autres analogues nucléosidiques antiviraux de cette étude étaient des antimétabolites, qui sont généralement utilisés pour le cancer ou l’immunosuppression. Ils ont testé l’activité antivirale de la tuberculidine, de la thioguanine et de la 6-mercaptopurine.
De plus, en testant l’effet de l’inhibition de la de novo biosynthèse des nucléotides, ils ont identifié un sous-ensemble d’inhibiteurs de la biosynthèse des pyrimidines et des purines. Ils ont également confirmé que la modification des pools de nucléosides peut bloquer avec succès la réplication virale. La synergie frappante signalée entre les inhibiteurs de la DHODH (Brequinar ou BAY-2402234) et les analogues nucléosidiques (Molnupiravir ou Remdesivir).
Lors des tests d’activité contre l’infection par des variantes du SRAS-CoV-2, les chercheurs ont noté que « la limitation du pool de pyrimidines en combinaison avec des antiviraux à action directe augmente l’activité antivirale des analogues nucléosidiques contre diverses souches de SARS-CoV-2 ».
De plus, les chercheurs ont testé des traitements combinés et ont trouvé une réduction robuste de la réplication virale lors de la co-administration de l’un des inhibiteurs de la DHODH (Brequinar ou BAY-2402234) et du Molnupirivir. Ils ont également confirmé ce in vivo rapport : une combinaison de Molnupiravir et de Brequinar réduit la réplication virale avec une pathologie diminuée dans les modèles murins.
« Le molnupiravir et le brequinar sont tous deux des médicaments administrés par voie orale qui font l’objet d’essais cliniques chez des patients COVID-19, et nous avons observé une activité antivirale synergique avec ces médicaments dans divers systèmes cellulaires modèles. »
Cette étude suggère que la combinaison de plusieurs traitements antiviraux pour supprimer l’infection virale peut être une méthode prometteuse pour traiter le COVID-19. La combinaison d’analogues nucléosidiques avec des inhibiteurs de la DHODH serait bénéfique, car la combinaison réduirait à la fois la réplication et l’inflammation dues à l’infection par le SRAS-CoV-2 dans les limites thérapeutiques, concluent les chercheurs.
Référence de la revue :
- Les inhibiteurs de la biosynthèse de la pyrimidine agissent en synergie avec des analogues nucléosidiques pour bloquer l’infection par le SRAS-CoV-2, David C. Schultz, Robert M. Johnson, Kasirajan Ayyanathan, Jesse Miller, Kanupriya Whig, Brinda Kamalia, Mark Dittmar, Stuart Weston, Holly L. Hammond, Carly Dillen, Lauren Castellana, Jae Seung Lee, Minghua Li, Emily Lee, Samuel Constant, Marc Ferrer, Christoph A. Thaiss, Matthew B. Frieman, Sara Cherry, bioRxiv 2021.06.24.449811; doi : https://doi.org/10.1101/2021.06.24.449811, https://www.biorxiv.org/content/10.1101/2021.06.24.449811v1

















