Une équipe de scientifiques des États-Unis a récemment défini l’enveloppe du substrat de la principale protéase du coronavirus 2 du syndrome respiratoire aigu sévère (SRAS-CoV-2). L’étude est actuellement disponible sur le bioRxiv* serveur de préimpression en attendant l’examen par les pairs.
Étude : Définition de l’enveloppe du substrat de la protéase principale du SRAS-CoV-2 pour prédire et éviter la résistance aux médicaments. Crédit d’image : Mark Umbrella/Shutterstock
Sommaire
Fond
Le SRAS-CoV-2, l’agent pathogène responsable de la maladie à coronavirus 2019 (COVID-19), est un virus à ARN enveloppé, à sens positif et simple brin de la famille des bêta-coronavirus humains. Le génome du SRAS-CoV-2 contient plusieurs polyprotéines qui sont clivées par des protéases virales pour libérer des protéines individuelles. La principale protéase virale joue un rôle crucial dans le clivage de ces sites, essentiel à la réplication virale. Ainsi, tous les médicaments antiviraux qui empêchent directement le clivage viral sont considérés comme de puissants inhibiteurs de la croissance virale. Dans ce contexte, des études cliniques portant sur l’efficacité antivirale des principaux inhibiteurs de protéase ont montré des résultats prometteurs.
Les protéases virales sont connues pour lier les sites de clivage des protéines avec diverses séquences d’acides aminés à travers une structure tridimensionnelle conservée (enveloppe du substrat). Par conséquent, les inhibiteurs viraux qui occupent le même espace que les substrats endogènes dans l’enveloppe du substrat sont moins susceptibles de développer une résistance due aux mutations virales.
Dans la présente étude, les scientifiques ont analysé neuf structures cocristallines à haute résolution de la protéase principale du SRAS-CoV-2 avec des sites de clivage viral pour définir la base structurelle de la reconnaissance du substrat.
Observations importantes
L’analyse de la structure cristalline de la protéase principale avec neuf substrats et six complexes de produits (structures de produits liées au côté N-terminal clivé du substrat) a révélé que les séquences de clivage naturelles ne sont pour la plupart pas conservées. Une conservation complète n’a été remarquée que pour la glutamine en position P1 et une leucine/phénylalanine/valine hydrophobe en position P2.
Les principales protéases virales se sont avérées cristalliser sous forme d’homodimère. Sur neuf complexes, six avaient un dimère dans l’unité asymétrique, les deux sites actifs étant occupés par un substrat. Les trois autres complexes avaient un monomère dans l’unité asymétrique.
Une analyse plus approfondie des structures cocristallines a révélé que le peptide substrat est étendu le long du site actif de la protéase principale avec la liaison scissile. Les résidus proches de la liaison scissile ont participé aux interactions moléculaires entre le substrat et la protéase principale. Alors que le côté N-terminal du substrat a montré une conservation complète dans toutes les structures, les résidus C-terminaux ont montré divers modes de liaison.
L’interaction substrat – protéase a été stabilisée par de multiples liaisons hydrogène qui se sont formées entre les peptides substrats et les principaux sites actifs de la protéase. Un vaste réseau de liaisons hydrogène squelette-squelette a été observé dans les structures, ce qui a déterminé la spécificité de substrat de la protéase principale.
Une analyse plus approfondie de la paire substrat-protéase a révélé que les résidus sur la surface du site actif de la protéase principale pouvaient tolérer une grande variété de mutations. Cependant, les interactions entre l’activité et le substrat sont restées essentiellement inchangées.
Enveloppe du substrat principal de la protéase SARS-CoV-2
En ce qui concerne la spécificité du substrat, la protéase principale s’est avérée reconnaître une forme conservée du substrat, malgré les différences de séquence. Cette forme conservée définit l’enveloppe du substrat de la protéase principale. L’analyse du site de clivage le plus conservé (substrats de protéines non structurelles 8 – 9) entre les coronavirus a révélé un ajustement parfait du site dans l’enveloppe du substrat. Certaines régions hautement conservées entre tous les complexes de substrats ont été identifiées malgré les différences dans les séquences d’acides aminés. Cette haute conservation détermine la spécificité des substrats.
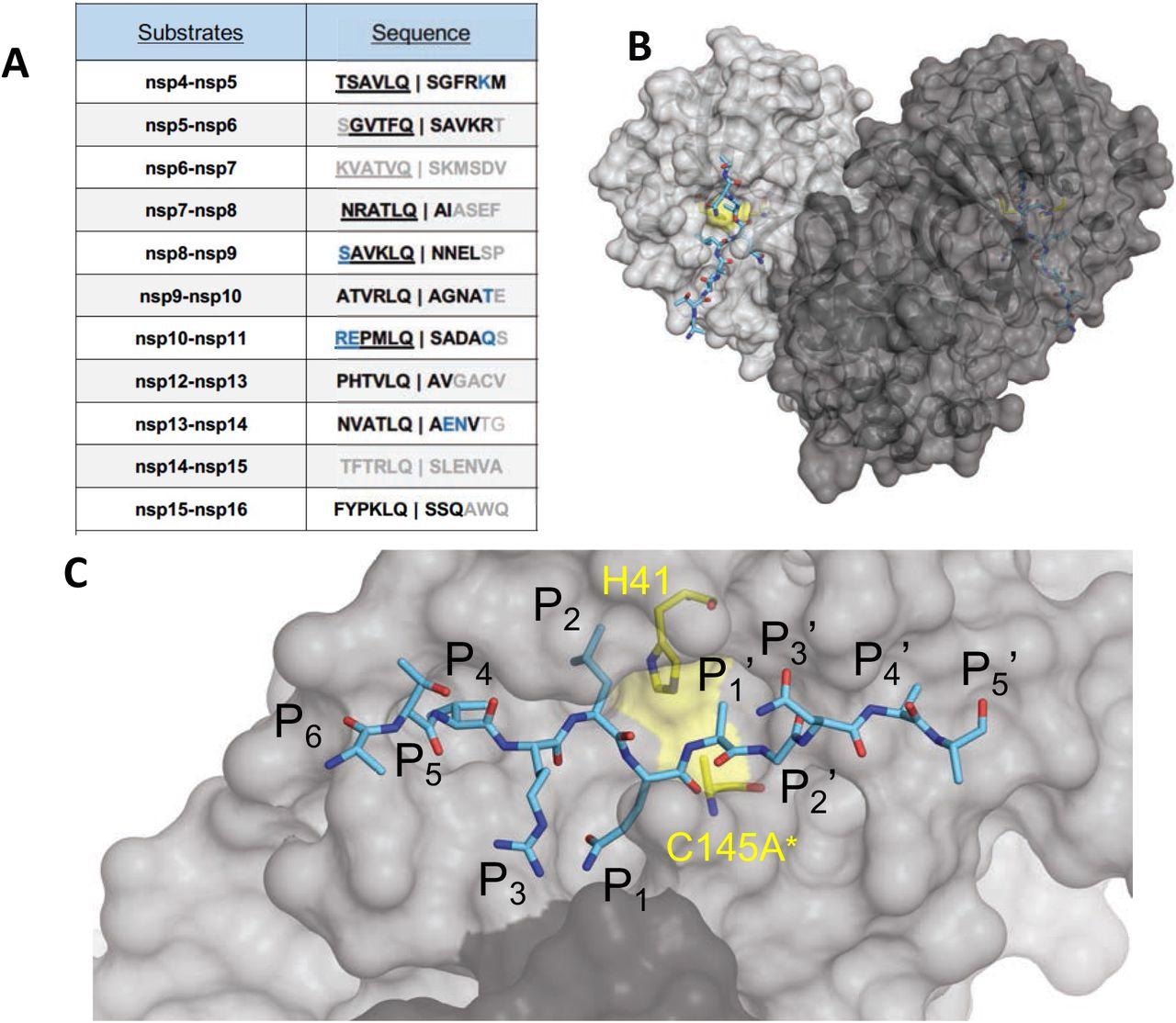
Les séquences d’acides aminés et la liaison des substrats au site actif SARS-CoV-2 Mpro. (A) Sites de clivage de polyprotéine virale traités par Mpro pour libérer des protéines non structurelles (nsp). Les codes d’acides aminés à une lettre des séquences de sites de clivage, où les lettres en gras indiquent des résidus entièrement résolus et le bleu sont des chaînes latérales tronquées dans les structures cocristallines. Les séquences N-terminales soulignées correspondent à des complexes de produits avec des structures cocristallines déterminées indépendamment. (B) Structure cristalline de SARS-CoV-2 Mpro avec un peptide substrat (nsp9-nsp10) lié au site actif des deux monomères (gris clair et plus foncé). Le peptide est représenté sous forme de bâtonnets cyan et la dyade catalytique est colorée en jaune. (C) Vue rapprochée de l’un des sites actifs dans le panneau B, avec la protéase en représentation de surface. L’astérisque indique que la cystéine catalytique a été mutée pour empêcher le clivage du substrat. Le clivage se produit entre les positions P1 et P1′.
Principaux inhibiteurs de la protéase et mutations de résistance
Les sites de séquence canonique (à l’extérieur de l’enveloppe du substrat) à partir desquels les inhibiteurs font saillie pour entrer en contact avec la protéase principale sont très vulnérables car les changements induits par la mutation dans ces sites peuvent potentiellement réduire la liaison de l’inhibiteur sans affecter la liaison au substrat et le clivage.
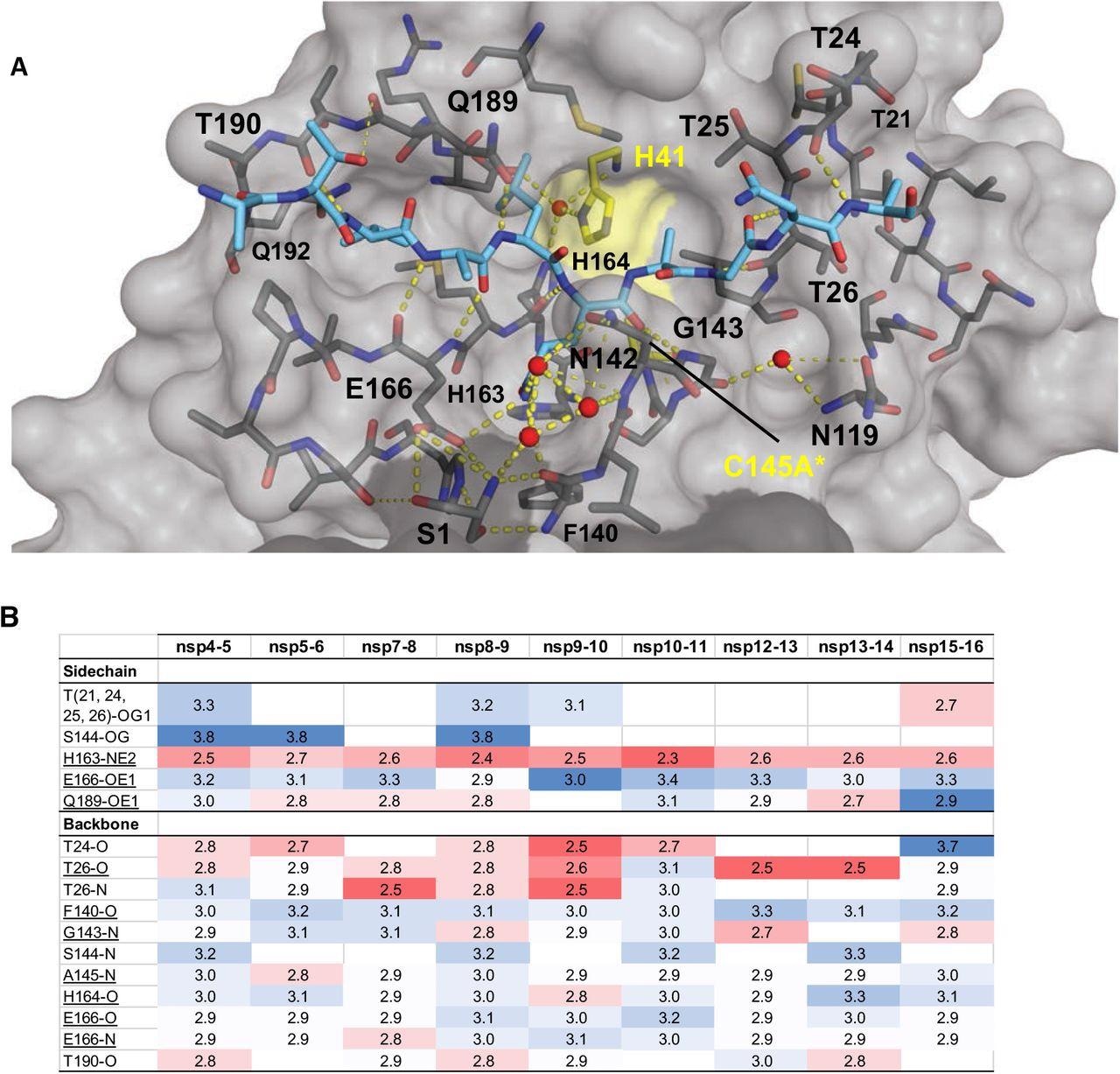
Liaisons hydrogène intermoléculaires dans les structures cocristallines du substrat Mpro. (A) Liaisons hydrogène entre le substrat nsp9-nsp10 lié et Mpro. Le peptide substrat est représenté sous forme de bâtonnets cyan et la protéase est en représentation de surface grise avec la dyade catalytique colorée en jaune. Les lignes pointillées jaunes indiquent des liaisons hydrogène (lignes plus épaisses pour des liaisons plus fortes avec une distance inférieure à 3,5 Å) et les sphères rouges indiquent des molécules d’eau conservées. Serl représenté sous forme de bâtons appartient à l’autre monomère (représenté en gris plus foncé). (B) Liaisons hydrogène qui sont conservées dans trois complexes de substrat ou plus, soulignées complètement conservées, en haut interagissant avec les chaînes latérales Mpro et en bas avec les atomes du squelette Mpro, codées par la proximité de la liaison hydrogène.
Quatre inhibiteurs principaux de la protéase du SRAS-CoV-2 ont été analysés dans l’étude, qui a révélé un schéma diversifié de liaison avec le site actif principal de la protéase. Les trois résidus les plus flexibles ont été identifiés, ce qui a montré des variations de conformation en fonction du type d’inhibiteur. Ces variations ont été principalement observées dans les sites de l’enveloppe du substrat où les inhibiteurs faisaient saillie. Ces sites n’étaient pas conservés parmi les coronavirus et pourraient servir de régions potentielles pour des mutations de résistance.
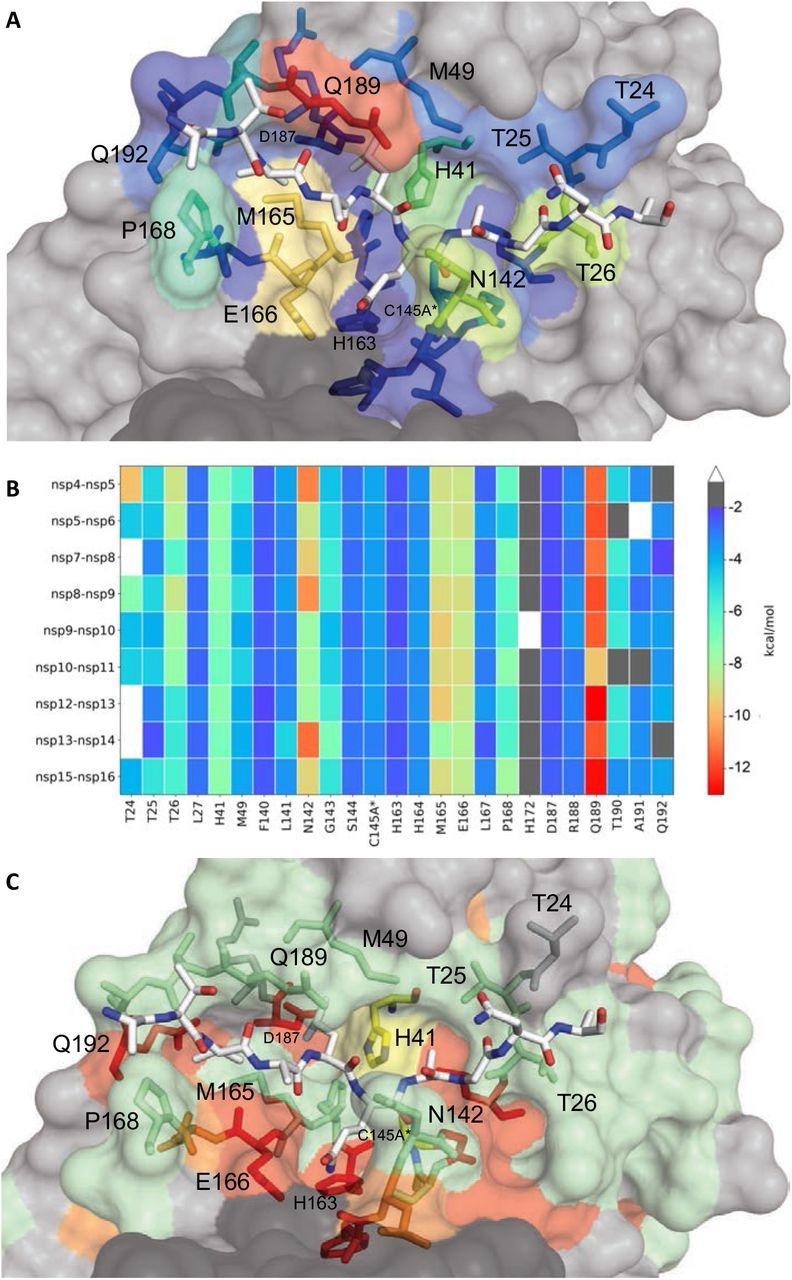
Étendue des interactions avec le substrat et conservation des résidus de surface Mpro. (A) Vue rapprochée du substrat nsp9-nsp10 lié au site actif Mpro dans la structure cocristalline où le peptide substrat est représenté sous forme de bâtons blancs et la protéase est en représentation de surface. Les résidus de protéase sont colorés en fonction de l’étendue des interactions de van der Waals avec le substrat, des couleurs plus chaudes indiquant plus d’interaction. (B) Conservation des interactions substrat-protéase van der Waals parmi les 9 structures cocristallines déterminées. Coloration de la carte thermique par l’étendue du contact de van der Waals par résidu. (C) Conservation de la séquence d’acides aminés de Mpro entre 7 (Figure S4) espèces coronavirales représentées sur la structure où les résidus de surface sont conservés dans les 7 (rouge), 5-6 (orange), 3-4 (vert) et moins de 3 ( très variable ; gris) les séquences sont indiquées par la couleur.
Importance de l’étude
L’étude décrit la base structurelle de l’interaction entre la protéase principale du SRAS-CoV-2 et ses substrats, c’est-à-dire les sites de clivage des protéines. De plus, l’étude révèle que les principaux inhibiteurs de protéase qui s’inscrivent dans l’enveloppe du substrat de la protéase principale sont moins susceptibles de développer une résistance car les mutations virales affectant la liaison de ces inhibiteurs altéreraient également la liaison entre la protéase principale et ses substrats.
*Avis important
bioRxiv publie des rapports scientifiques préliminaires qui ne sont pas évalués par des pairs et, par conséquent, ne doivent pas être considérés comme concluants, guider la pratique clinique/les comportements liés à la santé, ou traités comme des informations établies.[if–>