En décodant la structure et la fonction complexes de la barrière hémato-encéphalique, les chercheurs ouvrent la voie à de nouvelles thérapies capables de briser en toute sécurité les défenses les plus résistantes du cerveau.
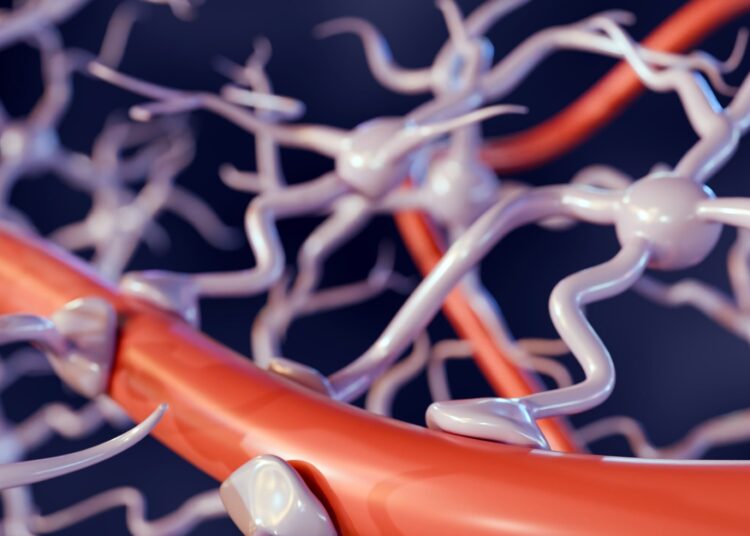
Introduction : La barrière hémato-encéphalique. Crédit d’image : Employé d’amour/Shutterstock
Dans un article récent publié dans la revue Biologie actuelleles chercheurs ont élucidé la structure et la fonction de la barrière hémato-encéphalique (BBB). Il met en évidence la BHE comme une interface complexe et dynamique qui sépare le système nerveux central (SNC) de la circulation sanguine somatique générale.
L'introduction établit également comment le dysfonctionnement de la BBB est un élément clé des maladies neurologiques telles que les accidents vasculaires cérébraux et la maladie d'Alzheimer. Il met en évidence des mécanismes supplémentaires de compromission des barrières dans le vieillissement et les maladies des petits vaisseaux cérébraux, ainsi que les avancées futures qui pourraient surmonter les limites actuelles des interventions neurologiques entravées par la sélectivité de la BBB.
Sommaire
Arrière-plan
Bien qu’il soit le centre de commande du corps, le cerveau est un organe incroyablement délicat. Alors que le crâne offre une protection physique contre les traumatismes externes, les menaces internes liées aux toxines véhiculées par le sang, aux agents pathogènes et aux cellules immunitaires activées nécessitent une approche défensive différente, la barrière hémato-encéphalique (BBB).
Découvert pour la première fois à la fin du XIXe et au début du XXe siècle, le BBB était traditionnellement perçu comme un mur presque entièrement imperméable. Cependant, les travaux pionniers de Lina Stern et Raymond Gautier ont remis en question cette notion, démontrant que la BHE pouvait être traversée par certaines substances et liant les effets cognitifs d'une substance à sa capacité à pénétrer la BHE.
Ces découvertes ont fait évoluer la vision scientifique du monde, passant d’une vision du BHE comme un mur à un filtre incroyablement sélectif (un concept médical désormais établi). Les premières études comparatives ont depuis montré que les structures de type BBB ont évolué indépendamment dans plusieurs lignées animales, depuis les barrières gliales chez les requins jusqu'aux barrières sans péricytes chez les lamproies, soulignant la diversité évolutive.
Le présent document de base répond à ces lacunes dans les connaissances en élucidant les avantages structurels et fonctionnels du BBB.
La structure de la barrière
Des décennies de recherche sur des modèles de rongeurs, d'autres vertébrés et des humains ont révélé que la BHE des mammifères est un système complexe à plusieurs couches, souvent appelé unité neurogliovasculaire, comprenant des cellules endothéliales, des péricytes, des membranes basales et des astrocytes travaillant de concert.
L’unité est composée de trois principaux types de cellules qui diffèrent radicalement dans leur structure et leur fonction :
Cellules endothéliales, qui sont « reliées » ensemble par des protéines comme la claudine-5 et l'occludine, formant ainsi une doublure protectrice le long des parois internes des capillaires sanguins du cerveau. Il a été observé que ces protéines forment des jonctions serrées qui limitent considérablement la diffusion paracellulaire (fuite de substances entre les cellules). Un glycocalyx endothélial luminal, un maillage riche en protéoglycanes, contribue à l'exclusion sélective de charge et est une des premières victimes du stress BBB, présageant une infiltration de leucocytes.
Cellules péricytaires, connues pour soutenir la fonction des cellules endothéliales en s'enroulant autour du vaisseau et en s'ancrant physiquement via de profondes invaginations « à chevilles et à douilles ». Il s’avère en outre que les péricytes fonctionnent indépendamment en tant que régulateurs essentiels de la stabilité et de l’intégrité des barrières.
Les astrocytes sont un type majeur de cellules gliales (de soutien) du cerveau. L'imagerie à haute résolution des astrocytes a permis d'observer que ces cellules possèdent des processus (appelés « pieds d'extrémité ») qui enveloppent le système vasculaire cérébral. Les pieds d'extrémité sont riches en aquaporine-4, un canal d'eau qui joue un rôle essentiel dans la régulation de l'homéostasie de l'eau et l'élimination des fluides pour prévenir l'œdème (gonflement du cerveau) et dans le maintien des gradients ioniques grâce à un échange coordonné Na⁺/K⁺.
Une exception importante concerne les organes circumventriculaires, où les vaisseaux fenêtrés permettent des échanges plus libres, tamponnés par des barrières immunitaires gliales plus profondes pour maintenir une communication contrôlée du SNC.
La fonction de la barrière
Un ensemble important de preuves a révélé que l’architecture BBB crée une barrière robuste à l’entrée d’éléments nocifs tout en permettant l’entrée et la sortie des nutriments essentiels (requis par le cerveau) et des déchets (ou molécules de signalisation), respectivement. Le transport sélectif a donc été décrit comme la fonction principale de la BHE, la transcytose médiée par les vésicules étant nettement réprimée par rapport à l'endothélium périphérique.
Des études mécanistiques ont démontré que le transport à travers la BBB s'effectue via plusieurs voies :
On sait que la diffusion passive de petits gaz lipophiles (liposolubles) comme l'oxygène (O₂) et le dioxyde de carbone (CO₂) se produit facilement à travers les membranes des cellules endothéliales.
La recherche a identifié une « superfamille de transporteurs de solutés » qui facilite le transport et qui fournit des canaux de transport BBB dédiés aux nutriments essentiels. Cela inclut le transporteur de glucose 1 (GLUT1), qui favorise l'absorption de plus de 100 grammes de glucose (par jour) pour répondre aux besoins métaboliques du cerveau. Un autre, MFSD2A, transporte l'acide docosahexaénoïque (DHA), un acide gras oméga-3 essentiel aux membranes neuronales. D'autres transporteurs, tels que l'OATP/SLCO1A2, transportent des produits thérapeutiques sélectionnés et des peptides endogènes à travers la BBB.
Il a été observé que le transport actif de grosses molécules, telles que l'insuline ou les lipoprotéines, utilise la transcytose médiée par les récepteurs. Plus précisément, ces molécules se lient à des récepteurs spécifiques à la surface cellulaire, qui internalisent ensuite la molécule dans une vésicule et la font circuler à travers la cellule. Les exemples incluent LRP1, qui fait le trafic des complexes lipoprotéiques et assure la médiation de la clairance amyloïde-β, et les récepteurs hormonaux tels que les récepteurs de l’insuline et de la leptine.
Le « pompage d'efflux » fait référence à des transporteurs qui pompent activement (en utilisant l'énergie cellulaire) des substances hors du cerveau. La mieux étudiée est la glycoprotéine P (P-gp), qui agit comme un « videur », utilisant de l'énergie (sous forme d'ATP) pour expulser un large éventail de xénobiotiques (substances étrangères) et de déchets métaboliques.
Conclusions
Le présent article explique la structure et la fonction de la BHE, en mettant en évidence le rôle du filtre dynamique dans l'entretien ménager et les mécanismes qu'il exploite pour maintenir l'homéostasie physiologique. Malheureusement, cela révèle également une limite : l'efficacité de la BBB à bloquer les xénobiotiques via des pompes à efflux comme la P-gp est une raison importante pour laquelle de nombreux médicaments prometteurs contre les troubles neurologiques ne parviennent pas à atteindre leurs cibles dans le cerveau.
La déficience de la BBB apparaît tôt dans le vieillissement et chez les porteurs de l'APOE ε4 et coexiste souvent avec une maladie des petits vaisseaux cérébraux, où les lésions microvasculaires chroniques et la perte de péricytes dégradent l'intégrité de la barrière.
Les états inflammatoires systémiques et les infections telles que le COVID-19 peuvent activer l’endothélium, réguler positivement les molécules d’adhésion et augmenter de manière transitoire la perméabilité, contribuant ainsi aux symptômes cognitifs.
Il est encourageant de constater que les recherches futures se concentrent sur le développement de modèles « d’organes sur puce » dérivés de patients afin de mieux étudier la BHE humaine et sur la conception de systèmes d’administration basés sur la nanotechnologie qui peuvent la traverser en toute sécurité et avec précision. La maîtrise de cette barrière est essentielle au traitement des maladies cérébrales les plus difficiles.