Les infections par le virus Zika sont devenues une épidémie locale dans les Amériques à divers moments dans le passé récent. Une étude récente a tenté d’explorer si cela était dû à des caractéristiques de transmissibilité accrues dues à une mutation ou à une recombinaison.
Étude : Les analyses génomiques et phénotypiques suggèrent des différences de fitness modérées entre les lignées de virus Zika. Crédit d’image : NIAID
Introduction
Le virus Zika a infecté environ 100 millions de personnes lors de l’épidémie de 2014 dans les Amériques. Il est connu pour provoquer une microcéphalie chez 7% des nouveau-nés nés de mères infectées pendant la grossesse, avec des anomalies neurologiques ou oculaires chez 6% supplémentaires.
Ces effets n’ont été signalés qu’à partir de ce moment. Cela a conduit à l’hypothèse que «le virus a acquis des mutations qui ont augmenté la virulence » et qu’il « adapté aux moustiques ou aux humains, ce qui a peut-être facilité sa propagation explosive à travers les Amériques.”
L’étude actuelle, publiée dans la revue PLOS Maladies Tropicales Négligéesvisant à explorer la possible adaptation phénotypique du virus Zika pour augmenter sa transmissibilité et sa virulence dans les Amériques.
Tout d’abord, les scientifiques ont analysé les séquences génomiques des virus Zika à partir d’un éventail d’échantillons prélevés lors de l’épidémie de 2015-16. Ensuite, ils ont identifié les lignées qui auraient pu émerger pendant cette période, en recherchant des différences de forme physique.
Les chercheurs ont également produit des courbes de croissance pour les lignées de virus Zika en utilisant douze virus Zika modifiés avec du matériel génétique recombinant pour représenter des lignées spécifiques du virus. Ces virus ont infecté des cellules humaines de plusieurs lignées, ainsi que des cellules vivantes Aedes aegypti les moustiques, qui sont le principal vecteur de ce virus.
De nombreux moustiques nourris avec des repas de sang infectieux contenant l’un des clades n’ont pas montré la présence du virus dans leur salive, peut-être parce que certains des clades avaient de faibles titres de virus, limitant la concentration de virus dans tous les repas de sang. Pour compenser, les chercheurs ont utilisé des injections intrathoraciques de chacun des 12 clades du virus Zika dans des moustiques femelles.
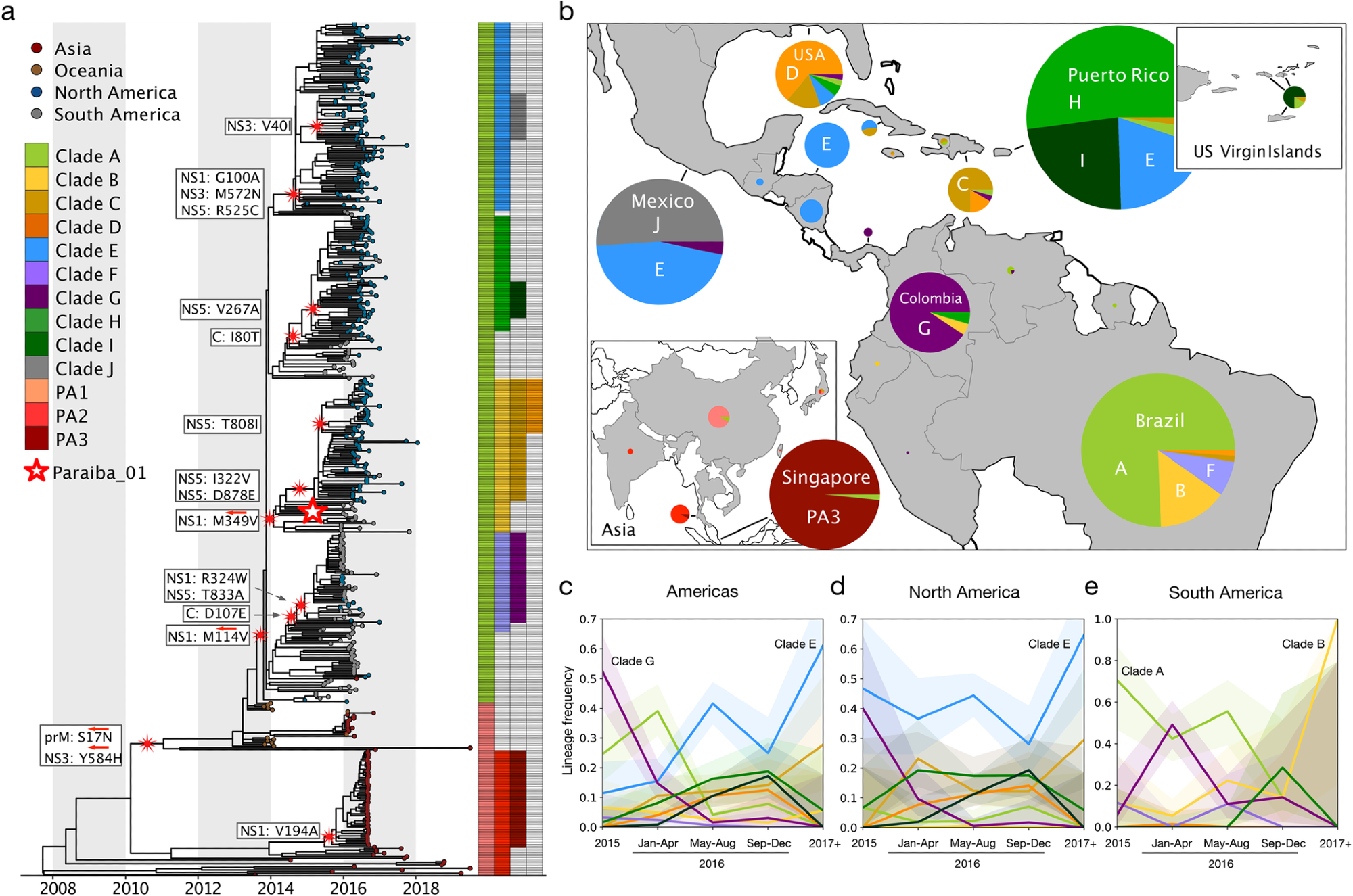
13 lignées majeures du virus Zika définies par des mutations non synonymes. (un) La phylogénie de Zika est divisée en 13 lignées définies par des mutations non synonymes. Grande étoile rouge et blanche : emplacement du clone infectieux initial dans lequel des mutations spécifiques ont été introduites. Cases blanches : mutations non synonymes introduites dans le clone infectieux initial pour modéliser chaque lignée. Flèches rouges : mutations non synonymes définissant la lignée qui sont revenues à leurs états ancestraux. (b) Proportions de clades circulant dans les pays des Amériques et d’Asie. Les tailles de tarte représentent le nombre de séquences. (Carte réalisée avec la carte de base des côtes de Natural Earth.) Fréquences temporelles des isolats de ZIKV séquencés à travers les Amériques (c)Amérique du Nord (y compris les Caraïbes et l’Amérique centrale) (d)Amérique du Sud (e) avec des intervalles de confiance à 95 %. Le point temporel 2015- représente les isolats collectés pendant ou avant 2015. Le point temporel 2017+ représente les isolats collectés pendant ou après 2017.
Qu’a montré l’étude ?
Les résultats de l’étude montrent que 13 clades significatifs peuvent être apparus au cours de l’épidémie de virus Zika de 2015-2016, trouvant finalement treize clades basés sur 17 mutations uniques. Parmi ceux-ci, le clade E semble avoir augmenté en fréquence, mais aucun n’était suffisamment dominant pour se fixer.
Les virus infectants ont donné naissance à deux lignées, le clade B et le clade E, avec une aptitude réplicative accrue après l’infection dans les cellules primaires humaines. Aucune divergence correspondante n’a été observée chez les moustiques infectés. Les deux méthodes d’infection par les moustiques n’ont montré aucune différence de transmission entre les clades.
Notamment, «aucune de nos lignées de virus Zika avec une aptitude réplicative améliorée n’a déplacé les lignées ancestrales pendant l’épidémie.”
L’aptitude réplicative accrue était associée aux mutations du clade E et du clade B, en particulier NS1-G100A, NS3-M572N et NS5-R525C dans le clade E et (NS1-M349V dans le clade B. L’association entre la mutation du clade E NS1-G100A et mieux la forme physique réplicative a déjà été rapportée par d’autres chercheurs dans des cellules de souris, mais son rôle correspondant dans les cellules humaines devrait être validé dans de futures études.
Le clade E se trouve dans la plupart des régions d’Amérique centrale, tandis que le clade B était une variante brésilienne précoce.
La substitution prM-S17N différencie la lignée PA2 du virus Zika du clade A mais ne confère pas explicitement de fitness ou de virulence au virus. Cependant, puisque la mutation NS3-Y584H définit également la lignée PA2, les effets indépendants de ces mutations sur le phénotype n’ont pas pu être analysés séparément dans cette étude.
Les chercheurs ont également identifié cinq sites de substitution d’acides aminés susceptibles de définir de nouvelles lignées et ont trouvé des preuves possibles de pressions de sélection positives. De manière significative, ils ont découvert que cela était vrai sur le site du clade B définissant la mutation NS1-M349V, ce clade présentant une aptitude réplicative élevée dans les cellules humaines.
La séparation des expériences de fitness dans les cellules humaines et les moustiques a exclu la possibilité d’analyser les changements de fitness réplicatif se produisant au cours d’un cycle naturel de transmission. Cependant, ils ont permis l’étude du parcours complet au cours duquel de nouvelles lignées ont émergé dans ces deux organismes. Certaines de ces lignées peuvent donc également être pertinentes dans la transmission naturelle, d’autant plus que les deux qui ont une meilleure aptitude réplicative n’ont aucun effet négatif dans l’une ou l’autre des lignées.
D’autre part, de nombreuses altérations phénotypiques spécifiques à certaines lignées ont été observées tout au long de l’épidémie de Zika, mais peu ont été fixées. Les deux lignées avec une forme physique accrue chez un hôte peuvent avoir une forme physique plus faible chez l’autre, ce qui limite leur survie et leur transmission. De plus, l’absence de mutations d’enveloppe dans les 13 lignées majeures identifiées dans cette étude suggère que l’évasion immunitaire ou les variantes d’évasion n’ont pas pris racine au cours de cette épidémie.
Quelles sont les implications ?
Deux lignées sont apparues lors de l’infection par les moustiques et les cellules humaines. Le mécanisme d’émergence des cinq lignées au cours de cette période semble être l’évolution adaptative. Fait intéressant, cela n’a pas conduit à la montée de lignées plus en forme déplaçant les moins en forme. Les études futures devraient examiner les résultats des mutations définissant ces lignées en ce qui concerne leurs effets phénotypiques.
L’importance fondamentale de ces lignées dans la survie et la transmission du virus Zika dans la nature reste à étudier en raison de la nature en laboratoire des expériences de cette étude. Cependant, le fort accord entre les différences de fitness réplicatif parmi toutes les lignées cellulaires humaines infectées par le virus suggère que ces effets peuvent bien se maintenir sur un large spectre de tissus humains.
« Pris ensemble, nos résultats suggèrent que si le virus Zika a probablement acquis des changements phénotypiques au cours de l’épidémie de 2015-2016 au fur et à mesure qu’il évoluait en réponse à de nouveaux environnements dans les Amériques, il est peu probable que ces changements aient eu un impact significatif sur le cours de l’épidémie..”
L’étude fournit un cadre de dépistage des différences de fitness au cours d’une épidémie et suggère plusieurs changements dans le phénotype viral au cours de cette période, mais sans effet significatif sur le cours de l’épidémie. Si ces changements peuvent être surveillés à ces moments-là, la propagation et la gravité de la maladie pourraient être atténuées plus facilement.
« Nous pensons que ce cadre peut être appliqué pour étudier l’évolution phénotypique lors de futures épidémies causées par des virus à ARN émergents.”

















