Les scientifiques pensent qu’une analyse impartiale des sites de liaison des anticorps fournirait des informations significatives sur la santé et les états pathologiques. À cet égard, de nombreux chercheurs ont utilisé des bibliothèques d’affichage de phages programmables pour détecter de nouveaux auto-anticorps. Des bibliothèques de présentation de phages ont été utilisées pour caractériser l’immunité antivirale et profiler des anticorps d’immunoglobuline E (IgE) spécifiques d’un allergène.
Même si les microréseaux de protéines sont extrêmement utiles pour la recherche sur les protéines, le coût élevé par test et les nombreux artefacts techniques les rendent moins conviviaux. Des technologies telles que le NAPPA (Nucleic Acid Programmable Protein Array) et l’expression in vitro à une seule molécule liée à la PCR (SIMPLEX) sont efficaces mais pas rentables.
Pour surmonter les limites du profilage basé sur un tableau de protéines de pleine longueur, les scientifiques ont développé une nouvelle méthodologie connue sous le nom d’analyse parallèle des cadres de lecture ouverts traduits (PLATO), basée sur l’affichage des ribosomes des bibliothèques de cadres de lecture ouverts (ORF). Cependant, certaines limites de PLATO ont entravé son acceptation massive dans la communauté scientifique.
Aujourd’hui, les scientifiques ont récemment développé une nouvelle technologie d’affichage moléculaire alternative appelée Indexation moléculaire des protéines par auto-assemblage (MIPSA). Leurs recherches, publiées sur le bioRxiv* serveur de pré-impression, explique comment cette technologie surmonte les inconvénients critiques de PLATO et d’autres technologies de matrice de protéines pleine longueur.
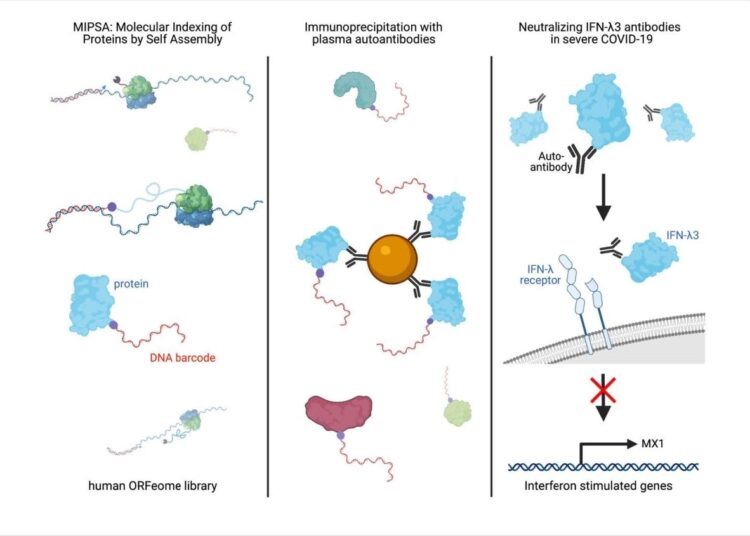
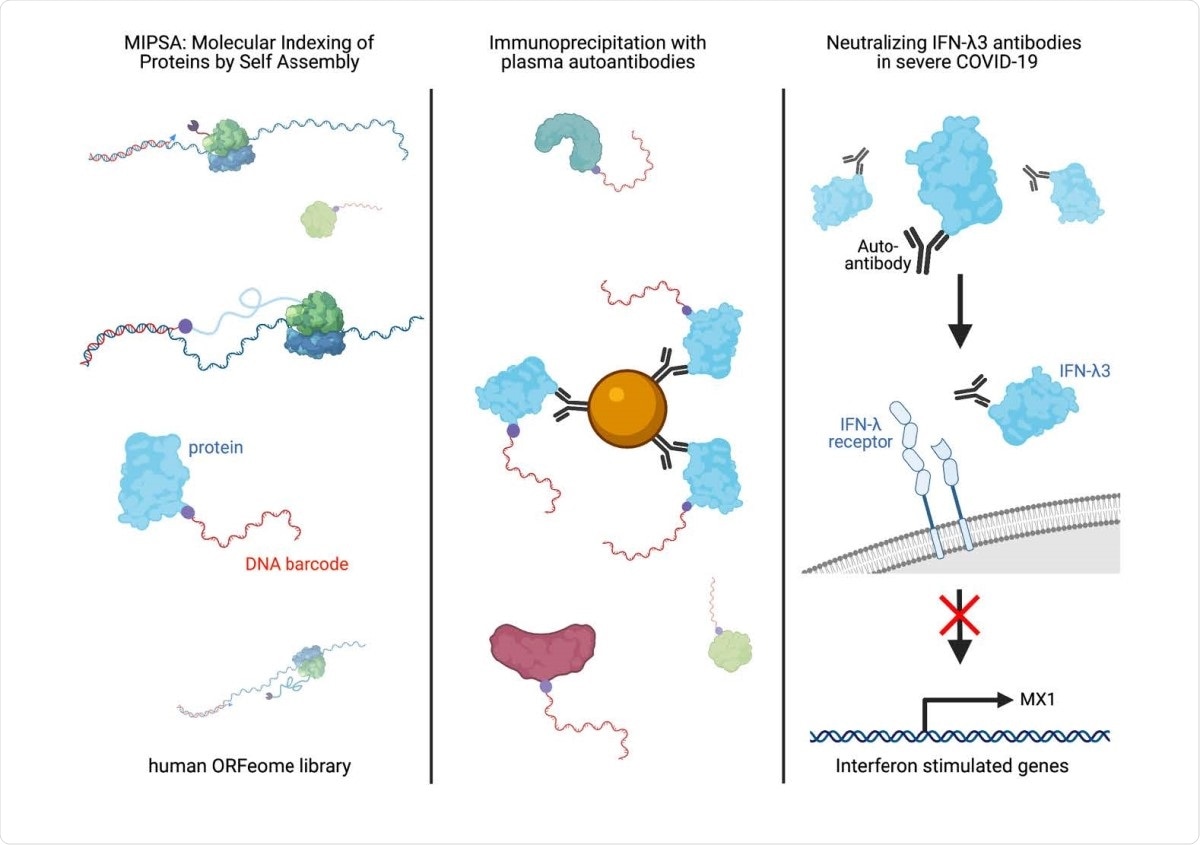
MIPSA produit des bibliothèques de protéines de pleine longueur solubles. Chaque protéine peut être identifiée explicitement par conjugaison covalente à un code-barres d’ADN bordé de séquences de liaison d’amorces PCR universelles. Les chercheurs ont incorporé les codes-barres à l’extrémité 5 ‘des séquences transcrites d’ARN messager (ARNm) qui sont positionnées en amont du site de liaison au ribosome (RBS). Un code-barres d’ADNc est produit par transcription inverse (RT) de l’extrémité 5 ‘de l’ARN transcrit in vitro (IVT-ARN) connecté à une amorce RT marquée par un haloalcane. Un HaloTag N-terminal est fusionné avec la protéine codée en aval du RBS. Ceci assure la traduction in vitro dans le couplage covalent intra-complexe («cis») du code-barres d’ADNc au HaloTag et à son produit protéique codé en cadre ouvert de lecture (ORF) en aval. Cette bibliothèque nouvellement formée contenant des protéines de pleine longueur indexées de manière unique peut être explorée dans de nombreuses études de protéome, par exemple, le profilage des auto-anticorps non biaisés. La recherche actuelle a dévoilé l’utilité de cette plate-forme en révélant la présence d’auto-anticorps connus et nouveaux dans le plasma de patients gravement atteints de COVID-19.
Un vecteur de destination MIPSA Gateway a été développé en utilisant plusieurs ingrédients vitaux. Il contient un site de départ de transcription de l’ARN polymérase T7, une séquence de code-barres isotherme identifiant clonal unique («UCI») flanquée de sites de liaison d’amorces constants, un site de liaison au ribosome (RBS), une protéine de fusion HaloTag N-terminale, des séquences de recombinaison pour l’insertion d’ORF , un codon d’arrêt et un site d’endonucléase d’origine pour la linéarisation du plasmide.
Le principal avantage de MIPSA par rapport à diverses autres technologies telles que les puces à protéines, SIMPLEX, NAPPA et PLATO est que ce système fournit un nouvel affichage moléculaire pour les protéines de pleine longueur. En outre, MIPSA offre une bibliothèque de séquençage simple, à haut débit et rentable qui assure la stabilité des complexes protéine-ADN. Ces attributs sont extrêmement bénéfiques à la fois pour la manipulation et le stockage des bibliothèques d’affichage.
MIPSA facilite les analyses impartiales des interactions protéine-anticorps, protéine-protéine et protéine-petite molécule. Il contribue également aux études de modification post-traductionnelle, par exemple, les études de modification des haptènes et le profilage de l’activité des protéases. En outre, cette technologie peut être facilement adoptée par les laboratoires de biologie moléculaire standard. En effet, il ne nécessite ni équipement ni formation sophistiqués. La disponibilité d’un simple instrument de séquençage d’ADN à haut débit est la seule exigence essentielle.
Même si le système d’affichage MIPSA utilise le système HaloTag / HaloLigand, il peut fonctionner avec l’étiquette SNAP formant une liaison covalente avec des dérivés de benzylguanine (BG). BG pourrait être utilisé comme étiquette pour l’amorce RT en remplacement de HaloLigand. MIPSA peut également prendre en charge le dérivé mutant du marqueur SNAP et le marqueur CLIP qui se lie aux dérivés O2-benzylcytosine.
Les scientifiques ont signalé l’association de l’auto-immunité avec la maladie grave du COVID-19. La recherche actuelle implique la détection de plusieurs auto-anticorps à l’aide du système d’affichage MIPSA. Chez les patients atteints d’une maladie COVID-19 sévère, des auto-anticorps neutralisants IFN-α / ω ont été rapportés. Ces auto-anticorps se produisent rarement dans la population générale et bloquent la réponse immunitaire à la réplication virale dans les cellules.
MIPSA complète des techniques comme PhIP-Seq. Une limitation de cette technologie est que le protocole MIPSA nécessite une traduction sans capuchon et sans cellule. On s’attend à ce que les travaux futurs aident à surmonter cet inconvénient. Dans l’étude actuelle, les scientifiques ont utilisé MIPSA pour détecter certains auto-anticorps connus et découvrir des auto-anticorps neutralisants de l’interféron lambda 3 (IFN-λ3).
En conclusion, les chercheurs suggèrent que l’autoréactivité de l’IFN-λ3 peut être plus fréquente chez les personnes atteintes de COVID-19 sévère. Il s’agit du premier rapport décrivant la neutralisation des auto-anticorps IFN-λ3 et propose donc un mécanisme pathogène potentiellement nouveau contribuant au COVID-19 potentiellement mortel chez un sous-ensemble de patients. Cette découverte aiderait à identifier les personnes qui présentent un risque plus élevé d’infection par le SRAS-CoV-2 et, par conséquent, à promouvoir l’utilisation thérapeutique de l’interféron-bêta dans ce groupe vulnérable.
*Avis important
bioRxiv publie des rapports scientifiques préliminaires qui ne sont pas évalués par des pairs et, par conséquent, ne doivent pas être considérés comme concluants, guider la pratique clinique / les comportements liés à la santé, ou traités comme des informations établies.
Référence du journal:
- Neutralisation des autoanticorps IFNL3 dans les COVID-19 sévères identifiés à l’aide de l’indexation moléculaire des protéines par auto-assemblage, Joel J.Credle, Jonathan Gunn, Puwanat Sangkhapreecha, Daniel R. Monaco, Xuwen Alice Zheng, Hung-Ji Tsai, Azaan Wilbon, William R. Morgenlander, Yi Dong, Sahana Jayaraman, Lorenzo Tosi, Biju Parekkadan, Alan N.Baer, Mario Roederer, Evan M. Bloch, Aaron AR Tobian, Israel Zyskind, Jonathan I. Silverberg, Avi Z. Rosenberg, Andrea L. Cox, Tom Lloyd, Andrew L. Mammen, H. Benjamin Larman, bioRxiv, 2021.03.02.432977; doi: https://doi.org/10.1101/2021.03.02.432977, https://www.biorxiv.org/content/10.1101/2021.03.02.432977v1