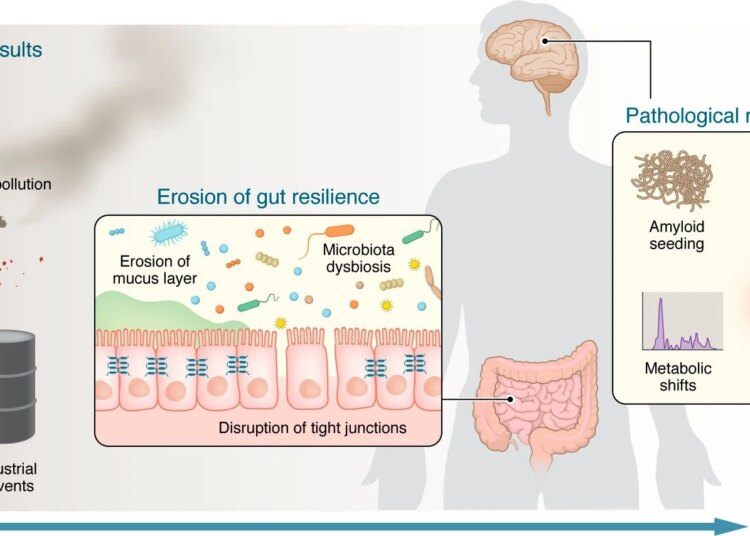
Les scientifiques suggèrent que la maladie de Parkinson pourrait commencer loin du cerveau, où les toxines environnementales, la perturbation du microbiome et les lésions de la barrière intestinale interagissent pour déclencher la cascade biologique menant à la neurodégénérescence.
Les agressions environnementales réduisent la résilience intestinale et déclenchent des mécanismes convergents à l’origine de la maladie de Parkinson. Toute une vie d’agressions environnementales (y compris les régimes alimentaires et additifs alimentaires occidentaux, les nano et microplastiques, les pesticides et herbicides, les solvants industriels et la pollution de l’air) agissent sur le microbiome et la barrière intestinale. Ces expositions favorisent la dysbiose du microbiote, perturbent les jonctions serrées et érodent la couche de mucus, réduisant collectivement la résilience intestinale. Une fois que cette défense périphérique est compromise, plusieurs voies mécanistiques propagent la pathologie au cerveau : (a) l’ensemencement amyloïde par des amyloïdes fonctionnels bactériens, (b) l’éducation inadaptée des lymphocytes T et les réponses auto-immunes, (c) les changements métaboliques induits par le microbiome qui génèrent des métabolites neurotoxiques et réduisent les acides gras à chaîne courte, et (d) l’amplification inflammatoire systémique. Ensemble, ces processus abaissent le seuil de mauvais repliement de l’α-syn, de la neuroinflammation et de la neurodégénérescence.
Une perspective récente publiée dans le Journal d'investigation clinique suggère que PD peut, chez certains individus, commencer dans l’intestin, en raison des expositions environnementales et des modifications du microbiome.
Sommaire
Augmentation de l'incidence de la maladie de Parkinson et des premiers symptômes non moteurs
L'incidence de PD a plus que doublé au cours de la dernière génération, les projections estimant une augmentation de plus de 50 % d’ici 2040. Cette augmentation dépasse ce qui peut s’expliquer par le vieillissement des populations, l’amélioration de la détection ou la seule génétique. PD se manifeste généralement par des symptômes moteurs progressifs, tels que rigidité, tremblements au repos, troubles de la marche et bradykinésie. Cependant, ces symptômes n’apparaissent qu’après une dégénérescence importante des neurones dopaminergiques de la substance noire, souvent après la perte d’environ la moitié de ces neurones.
Les symptômes prodromiques, notamment l'anosmie, les troubles du comportement en sommeil à mouvements oculaires rapides et la constipation, précèdent les symptômes moteurs de 10 à 20 ans. Étant donné que les changements pathologiques apparaissent en périphérie bien avant de se produire dans le cerveau, il faudra regarder au-delà du système nerveux central pour comprendre la charge croissante de morbidité. Ainsi, les auteurs proposent que l’intestin puisse agir comme une interface précoce où les expositions environnementales interagissent avec la biologie de l’hôte, plutôt que le cerveau seul soit le site de PDle développement initial de.
Expositions environnementales et érosion de la résilience de l'hôte
Les expositions environnementales, y compris les solvants (par exemple, le trichloréthylène), la pollution atmosphérique et les pesticides (par exemple, la roténone, le paraquat), sont impliquées dans PD pathogénèse. Pourtant, les expositions individuelles ne peuvent pas expliquer pleinement l’incidence croissante des PDce qui suggère que la maladie pourrait résulter de pressions environnementales cumulatives réduisant la résilience de l'hôte. Les auteurs proposent que l’intestin module la résilience grâce à l’intégrité de la barrière épithéliale ainsi qu’à la fonction et à la composition microbiennes.
Les toxines exercent une pression sélective, favorisant les taxons présentant des caractéristiques qui confèrent un effet néfaste. Par exemple, le paraquat produit des espèces réactives de l’oxygène (ROS), qui diminuent la diversité microbienne et enrichissent les entérobactéries qui génèrent des amyloïdes fonctionnels appelés curli. De même, le trichloréthylène inhibe le complexe mitochondrial I tout en restructurant le microbiote pour favoriser les bactéries sulfato-réductrices, par exemple Desulfovibrio, par rapport aux taxons neuroprotecteurs producteurs d'acides gras à chaîne courte.
Plusieurs facteurs environnementaux peuvent également perturber la barrière intestinale. Les émulsifiants alimentaires, par exemple le polysorbate-80 et la carboxyméthylcellulose, érodent la couche de mucine et affaiblissent la barrière. De plus, les microplastiques et les particules fines ingérés (PM2,5) compromettent la fonction barrière et déclenchent une inflammation. Ces particules concentrent également les pesticides et les métaux lourds à leur surface, facilitant ainsi le transport des toxines environnementales à travers la barrière intestinale.
Modifications du microbiote intestinal et mécanismes neurodégénératifs
Les entérobactéries contribuent à la pathologie de l'α-synucléine en générant des sous-unités curli (CsgB et CsgA). Ces amyloïdes sont structurellement similaires à l'α-synucléine. Curli peut accélérer l’accumulation d’α-synucléine et constitue également un modèle moléculaire associé à un agent pathogène qui stimule l’inflammation. Ce double rôle fait du curli un lien important entre les expositions environnementales et la neurodégénérescence. De plus, la dysbiose intestinale oriente le métabolisme vers différentes voies neurotoxiques.
Le commutateur de la kynurénine régule positivement l'indoleamine 2,3-dioxygénase, détournant le métabolisme du tryptophane de la synthèse de la sérotonine vers les neurotoxines dérivées de la kynurénine. Pendant ce temps, les bactéries sulfato-réductrices produisent un excès de sulfure d’hydrogène, qui inhibe la cytochrome c oxydase mitochondriale (complexe IV), altère la fonction mitochondriale et exacerbe l’accumulation d’α-synucléine. La perte d’acides gras à chaîne courte, comme le butyrate, aggrave encore ces changements.
Activation immunitaire reliant le dysfonctionnement intestinal à la dégénérescence cérébrale
Par conséquent, le dysfonctionnement de la barrière permet la translocation des composants bactériens dans la circulation systémique, où la détection immunitaire innée via les récepteurs Toll-like (TLR2 et TLR4) peut activer l'inflammasome NLRP3 et déclencher la libération d'interleukine (IL)-18 et IL-1β. Ces cytokines traversent la barrière hémato-encéphalique et amènent les microglies dans un état hyperréactif. Une fois amorcées, les microglies présentent des réponses exagérées aux agressions ultérieures provenant d'agrégats endogènes d'α-synucléine, d'infections virales ou de toxines exogènes de faible niveau.
Les auteurs soulignent également le rôle potentiel de l’éducation immunitaire intestinale, dans laquelle les CD4 réactifs à l’α-synucléine+ Les lymphocytes T peuvent être amorcés dans l’intestin avant de migrer vers le cerveau, où les réponses T auxiliaires pro-inflammatoires, notamment l’activité Th1 et Th17 et les cytokines telles que l’interféron-γ, pourraient contribuer aux lésions des neurones dopaminergiques.
Conclusions et implications pour la prévention de la maladie de Parkinson
Si PD résulte d’une vie de pression environnementale, alors les interventions efficaces doivent se concentrer sur le renforcement de la résilience biologique et la réduction de la charge environnementale. La recherche s'est concentrée sur le centre PD mécanismes depuis des décennies : dysfonctionnement mitochondrial, agrégation de l’α-synucléine, vulnérabilité des neurones dopaminergiques et neuroinflammation. Même si ces cibles restent essentielles, elles représentent des processus pathologiques en aval.
Au moment où ils sont détectables dans le cerveau, la maladie a peut-être déjà franchi un point d’inflexion crucial. En revanche, l’intestin est l’endroit où les expositions environnementales se croisent avec l’hôte. C’est là que l’intégrité de la barrière épithéliale et l’écologie microbienne déterminent si la tolérance immunitaire est érodée, si des graines d’α-synucléine mal repliées se forment et si l’inflammation systémique prépare le cerveau à la dégénérescence.
Dans l'ensemble, l'intestin représente une cible potentiellement modifiable sur le plan clinique dans PDqui est mécanistiquement en amont et thérapeutiquement accessible même après l'apparition de la maladie, les premières études suggérant des améliorations de certains symptômes et marqueurs biologiques, mais pas une inversion définitive de la maladie. Il peut donc être essentiel d’avancer vers l’amont pour inverser la tendance mondiale. PD tendances. Le renforcement de la résilience périphérique est l’une des stratégies les plus prometteuses, scientifiques et évolutives. Empêcher l'initiation dans l'intestin peut à terme contribuer à modifier PDla trajectoire.