Oncotarget a publié « Rôle pour Fgr et Numb dans la différenciation induite par l’acide rétinoïque et l’arrêt G0 des cellules AML non APL », qui a signalé que l’acide rétinoïque est un régulateur fondamental du cycle cellulaire et de la différenciation cellulaire.
À l’aide d’un modèle in vitro dérivé d’un patient leucémique d’une LAM non APL, ces auteurs ont précédemment découvert que la PR provoque l’activation d’un complexe de signalisation macromoléculaire, un signalosome, constitué de nombreuses molécules de signalisation liées à la voie MAPK ; et cette signalisation a permis aux éléments de réponse à l’acide rétinoïque de réguler l’expression génique qui entraîne la différenciation cellulaire/l’arrêt du cycle cellulaire. Vers un aperçu mécaniste de la nature de cette nouvelle signalisation, ils découvrent maintenant que la protéine déterminante du destin cellulaire NUMB est un échafaudage apparent pour le signalosome.
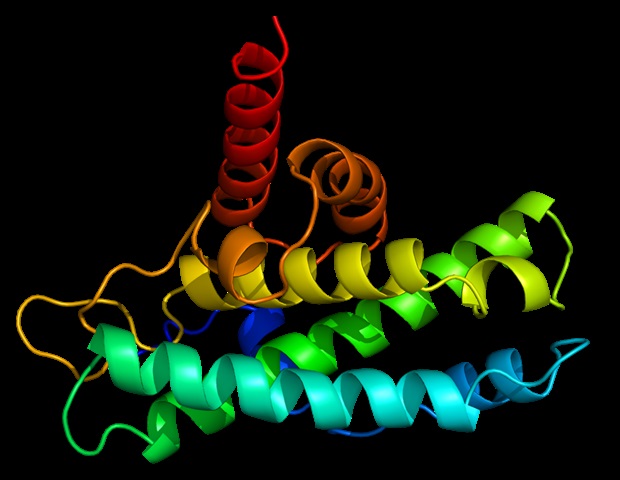
Numb existe dans la cellule liée à un ensemble de molécules de signalosome, y compris Raf, Lyn, Slp-76 et Vav.
Fgr se lie à NUMB, qui est associé à la phosphorylation de NUMB et à la liaison et à la phosphorylation améliorées de NUMB de certains composants du signalosome, trahissant ainsi l’activation du signalosome.
L’activation du signalosome est associée à la différenciation cellulaire le long de la lignée myéloïde et à l’arrêt du cycle cellulaire G1/0. Si l’expression de Fgr induite par la PR est supprimée par un CRISPR-KO ; ensuite, la phosphorylation de NUMB induite par la RA et la liaison et la phosphorylation améliorées de NUMB de certains composants du signalosome sont perdues. Les cellules ne parviennent plus à subir une différenciation induite par la PR ou un arrêt G1/0. En résumé, cette équipe de recherche a découvert que NUMB agit comme un échafaudage pour une machine de signalisation qui fonctionne pour propulser la différenciation induite par la PR et l’arrêt G1/0, et que Fgr se liant à NUMB active la fonction.
L’acide rétinoïque (AR) est un régulateur biologiquement fondamental de la prolifération et de la différenciation cellulaire. Il est conservé au cours de l’évolution et a des effets étendus dans de nombreux tissus. »
Dr Andrew Yen, Université Cornell
Il a été découvert que l’activation transcriptionnelle par RAR/RXR pour contrôler la différenciation cellulaire et l’arrêt du cycle cellulaire nécessite une signalisation liée à la voie MAPK pour permettre l’activation transcriptionnelle nécessaire pour conduire la différenciation cellulaire/l’arrêt du cycle cellulaire G1/0.
La principale découverte est que la protéine déterminante du destin Numb semble agir comme un échafaudage pour le signalsome, liant une « colonne vertébrale » de molécules à laquelle toutes les autres molécules signalsome sont attachées; et que RA a induit l’expression du Fgr SFK et sa liaison à Numb avec phosphorylation> de Numb, ainsi que d’autres événements de phosphorylation importants, indiquant l’activation du signal.
SLP-76 est phosphorylé avec le Fgr induit par la RA dans le poids parental, mais pas dans les cellules Fgr KO ; ainsi, la phosphorylation de Slp-76, l’une des phosphorylations de p-tyr induites par la RA les plus importantes, où Slp-76 est connue pour IP avec Fgr et Lyn, est également associée à la liaison de Fgr à Numb.
Numb se lie également à Lyn, qui est connu pour devenir Y416 phosphorylé avec le traitement RA; indiquant que la liaison à Fgr Numb est associée à la phosphorylation de Lyn, où Slp-76 et Lyn sont les associés les plus proches de Fgr dans la représentation du nœud de force signalétique des partenaires IP connus.
En somme, les données d’Oncotarget soutiennent un paradigme dans lequel les molécules de signalisation liées à un échafaudage Numb dans un signalsome sont activées par l’expression de Fgr induite par la PR et sa liaison à Numb pour propulser la différenciation induite par la PR et l’arrêt G1/0. Essentiellement, RA augmente ergo la quantité de signal et augmente la quantité de Fgr pour les activer, poussant ainsi la cellule à se différencier.
L’équipe de recherche Yen a conclu dans ses résultats de recherche Oncotarget qu’un défi majeur pour la thérapie de différenciation de la PR est l’émergence d’une résistance à la PR après le traitement initial de la PR.
Dans une tentative pour mieux comprendre comment il se développe, les cellules HL-60 résistantes à la PR ont été dérivées par culture soutenue dans des concentrations progressivement croissantes de PR.
Une étude de l’expression de molécules candidates potentiellement responsables a révélé que la plus grande divergence entre les cellules parentales et les dérivés résistants à la PR était l’échec des cellules résistantes à réguler à la hausse Fgr en réponse à la PR.
L’utilisation de médicaments au lieu de Fgr pour activer le signalsome en combinaison avec la PR peut donc être un moyen de surmonter la résistance.
Ainsi, le paradigme présenté ici peut fournir des informations sur les candidats, dont les dysfonctionnements sont déterminants pour la résistance.