Du régime méditerranéen aux métabolites microbiens, les scientifiques révèlent comment le maintien de la santé intestinale pourrait être une stratégie puissante pour retarder ou prévenir la maladie d'Alzheimer.
Revue: Diversité microbienne et forme physique dans l'axe intestinal-cerveau: influences sur le risque de développement de la maladie d'Alzheimer. Crédit d'image: Volodimir Zozulinskyi / Shutterstock
Dans une revue récente dans le journal Microbes intestinauxles chercheurs de l'Université de Gachon, République de Corée, résument plus de 110 publications scientifiques pour élucider le rôle de l'axe du cerveau intestinal dans le maintien de la santé gastro-intestinale. L'examen définit et élabore sur l'axe, en se concentrant sur la façon dont la santé microbienne intestinale optimale peut empêcher les conditions neurodégénératives telles que la maladie d'Alzheimer (AD). Il met en évidence à la fois les avancées scientifiques récentes dans le domaine et les lacunes dans la littérature et comment les technologies omiques de nouvelle génération peuvent combler ces lacunes, améliorant la santé publique dans le monde entier.
Sommaire
Arrière-plan
Le tractus gastro-intestinal (GI) héberge environ 80% des 100 billions de bactéries dans le corps humain, contenant des centaines ou même des milliers d'informations génétiques bactériennes plus que nos propres génomes. Le microbiome intestinal comprend principalement des bacteroidetes et des firmicutes, aux côtés de plus petites populations d'actinomyces, de protéobactéries, de verrucomicrobie et de fusobacterium, formant un écosystème unique qui régit la santé de l'hôte.
La recherche met l'accent sur l'importance de la communication à l'hôte du microbiome, réalisée via des composés de signalisation chimique appelés molécules de détection de quorum (QSMS). Ces QSM sont cruciaux pour l'axe du microbiote-intestin (MGBA), mais peuvent également favoriser la virulence dans les agents pathogènes comme Pseudomonas aeruginosa. Les modèles animaux sans germes montrent que l'élimination du microbiote gastro-intestinal et du QSMS conduit à des défauts neurodéveloppementaux, à une motilité gastrique anormale et à une immunité affaiblie, mettant en évidence leur rôle dans la digestion et la santé globale.
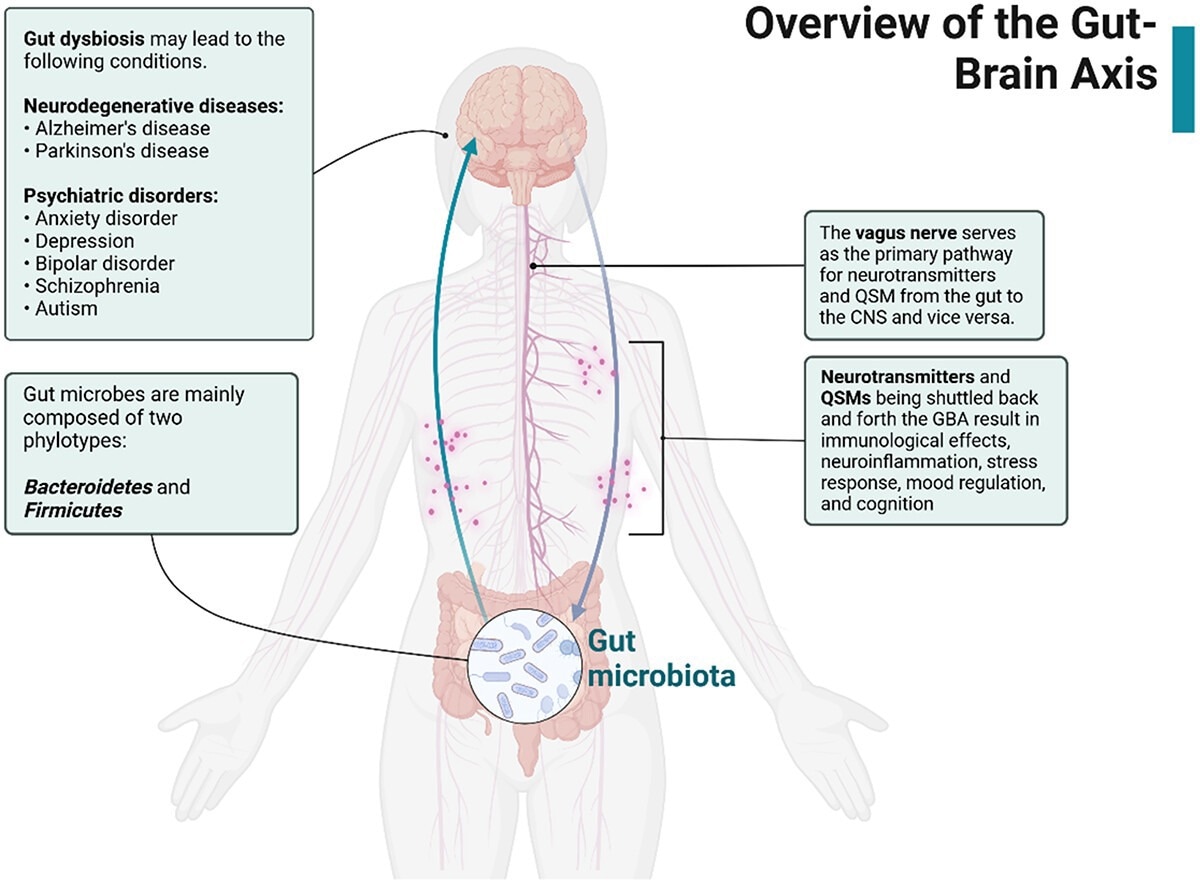
Présentation de l'axe intestinal-cerveau. Les microbes intestinaux libèrent les neurotransmetteurs et les QSM qui voyagent dans le nerf vague et influencent le SNC. En cas de dysbiose intestinale, des troubles neurodégénératifs peuvent survenir en raison de la réponse au stress, de la réponse immunologique et de la neuroinflammation. Créé avec biorender.com.
Communication en cerveau intestinal
Le MGBA relie le système nerveux central (SNC), les cellules digestives, le système nerveux entérique (ENS) et les microbes intestinaux, médiant la communication bidirectionnelle à travers diverses amines et peptides. Bien que complexes et non comprises, les modèles animaux ont montré leur importance dans le maintien de l'homéostasie et du bien-être.
La dysbiose intestinale, les altérations des populations microbiennes, a été liée à des comportements anxieux, à une sociabilité réduite, à des problèmes cognitifs et à des réponses au stress atypique. Les études de vagotomie soulignent le rôle du nerf vague dans la transmission des signaux entre l'ESS et le SNC.
Les QSM influencent l'expression des gènes dans les microbes et les hôtes, facilitant la communication et supprimant les bactéries nocives – mais certains permettent des traits pathogènes comme la formation de biofilm. Ces molécules régulent le comportement du microbiome et les processus critiques comme la production antimicrobienne et l'équilibre symbiotique. Certains QSM, comme les acides gras à chaîne courte (SCFA) et les indoles, interagissent avec les cellules hôtes pour influencer l'immunité et la fonction neurologique.
«Cette interférence avec le développement d'autres micro-organismes à travers des enzymes de quorum et des molécules auto-inductives antagonistes était notable. Il a mis en évidence les subtilités des microbes et des réseaux de communication dynamiques, qui employaient diverses stratégies pour gagner un avantage concurrentiel au sein de leurs communautés.»
Endocrinologie
Alors que certains QSM aident à la communication à hôtes microbes, la plupart fonctionnent entre les populations bactériennes. Les principales molécules communicatives entre l'intestin et l'hôte comprennent la sérotonine, le GABA et la dopamine.
Les changements dans la composition du microbiome peuvent entraver la synthèse de ces molécules essentielles, contribuant à la dépression et à l'anxiété dans les études animales et humaines. Les neuromodulateurs affectent la santé du cerveau par interaction directe avec les récepteurs gastro-intestinaux ou en entrant dans la circulation sanguine et en traversant la barrière hémato-encéphalique.
Dysbiose et avancées dans les techniques moléculaires
Des technologies de séquençage comme la protéomique, la transcriptomique et la métagénomique ont élargi notre compréhension du rôle du microbiome dans la santé.
Des études nutritionnelles montrent que des régimes comme le régime méditerranéen et le jeûne intermittent (IF) soutiennent la santé intestinale, tandis que les régimes occidentaux favorisent les déséquilibres microbiens et augmentent les risques pour l'inflammation, les troubles neurologiques et le cancer. Si cela s'est révélé prometteur en remodelant les communautés intestinales et en réduisant les plaques amyloïdes-bêta associées d'Alzheimer.
«Gupta et al. Développement de l'indice de santé du microbiome intestinal (GMHI), un algorithme prédisant la probabilité de la maladie à partir de la composition microbienne. À partir de 4 347 échantillons de selles humains, 50 espèces microbiennes bénéfiques ont été identifiées. Un GMHI 2 mis à jour comprenait 8,069 échantillons de 54 études globales, affinant les prédictions spécifiques aux maladies.» ».
Des recherches alimentaires à long terme montrent que des régimes sains comme le régime méditerranéen et si peuvent supprimer la neuroinflammation et réduire le risque de maladie d'Alzheimer. En revanche, les régimes occidentaux peuvent aggraver la progression de la maladie en altérant la barrière hémato-encéphalique et en favorisant l'inflammation.
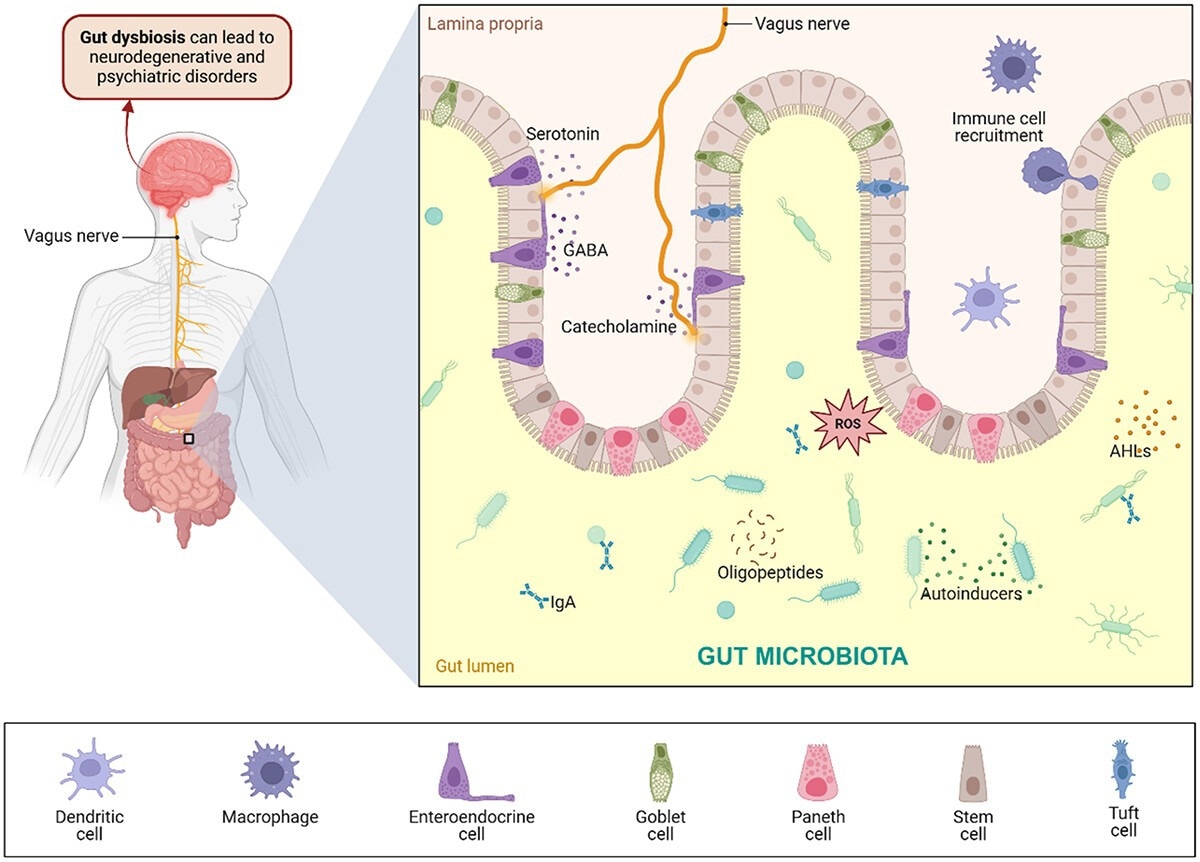
Cross-Kingdom Signalisation dans le GBA. Le microbiote intestinal libère plusieurs neuromodulateurs, tels que les neurotransmetteurs, les oligopeptides et d'autres métabolites, interagissant avec les cellules épithéliales et immunitaires. Les cellules spécialisées qui bordent l'épithélium intestinal maintiennent l'homéostasie intestinale, forment une barrière de mucus et facilitent le passage du matériau à travers les intestins. Les neurones reconnaissent également les neurotransmetteurs, qui voyagent dans le nerf vague jusqu'au cerveau. La dysbiose intestinale résultant de populations microbiennes intestinales déséquilibrées entraîne des effets immunologiques et de la neuroinflammation, entraînant éventuellement des troubles neurodégénératifs et psychiatriques. Créé avec biorender.com.
Conclusions
Le MGBA est vital pour la santé, influençant les risques pour diverses maladies. À mesure que la compréhension des interactions bactéries intestinales s'approfondissait, de nouvelles interventions cliniques peuvent émerger pour lutter contre la charge croissante des maladies non transmissibles et infectieuses.