Une étude récente dans le domaine de l’analyse des fluides révèle un ensemble diversifié de stratégies utilisées par les variantes alpha et bêta du coronavirus 2 du syndrome respiratoire aigu sévère (SRAS‑CoV‑2) afin d’échapper aux anticorps générés lors d’une infection antérieure par ce virus. Le document est actuellement disponible sur le bioRxiv* serveur de préimpression pendant qu’il est soumis à un processus d’examen par les pairs.
L’émergence de variantes préoccupantes du SRAS-CoV-2 – principalement le B.1.1.7 britannique (connu sous le nom de variante alpha) et la variante sud-africaine B.1.351 (connue sous le nom de variante bêta) – ont soulevé de graves inquiétudes quant aux mutations de leur glycoprotéine de pointe. Les séquences amélioreront la transmission et généreront une résistance à de multiples anticorps neutralisants.
Par conséquent, comprendre les facteurs exacts qui permettent l’échappement des anticorps du SRAS-CoV-2 et de ses variantes, connus pour provoquer la maladie à coronavirus 2019 (COVID-19), est essentiel pour le développement de médicaments et de vaccins efficaces qui offriront une large protection.
Les résultats du séquençage ont montré que les variants alpha et bêta du SRAS-CoV-2 partagent une mutation N501Y qui joue un rôle central dans l’interaction entre la glycoprotéine virale de pointe et le récepteur de l’enzyme de conversion de l’angiotensine 2 (ACE2) dans les cellules humaines.
Contrairement à la variante alpha, la variante bêta abrite des mutations E484K et K417N supplémentaires au niveau de la partie clé de la glycoprotéine de pointe connue sous le nom de domaine de liaison au récepteur (RBD), soulevant des préoccupations supplémentaires liées à la fuite d’anticorps viraux.
En utilisant le dimensionnement diffusionnel microfluidique, un groupe de recherche dirigé par le Dr Sebastian Fiedler du Royaume-Uni a résolu la constante de dissociation pour l’interaction entre les RBD du SARS-CoV-2 dans sa version originale (également connue sous le nom de virus de type sauvage) et ses alpha et variantes bêta avec le récepteur de la cellule hôte ACE2.
Sommaire
Une nouvelle approche pour l’évaluation de l’affinité des anticorps
Dans cette étude, les chercheurs ont utilisé des RBD de type sauvage, alpha et bêta pour quantifier l’impact de diverses mutations dans cette région exacte (plus précisément, des mutations telles que N501Y, E484K et K417N) sur l’affinité de liaison à ACE2 et une neutralisation monoclonale anticorps dirigé contre le Wuhan-Hu-1 SARS-CoV-2 original.
De plus, ce groupe de recherche a évalué les mêmes RBD de type sauvage et variant dans le processus connu sous le nom de profilage d’affinité des anticorps microfluidiques. Cela a été fait pour évaluer l’affinité et les concentrations d’anticorps anti-RBD dans les sérums de convalescence d’individus infectés par la variante originale du SRAS-CoV-2.
Une telle approche leur a permis de discerner les changements d’affinité dans l’ensemble de la population d’anticorps en évaluant la perte de liaison dans un sous-ensemble d’anticorps. De plus, ils ont poursuivi une analyse de corrélation de ces affinités et concentrations avec la propension à perturber les complexes entre le récepteur et la glycoprotéine de pointe virale.
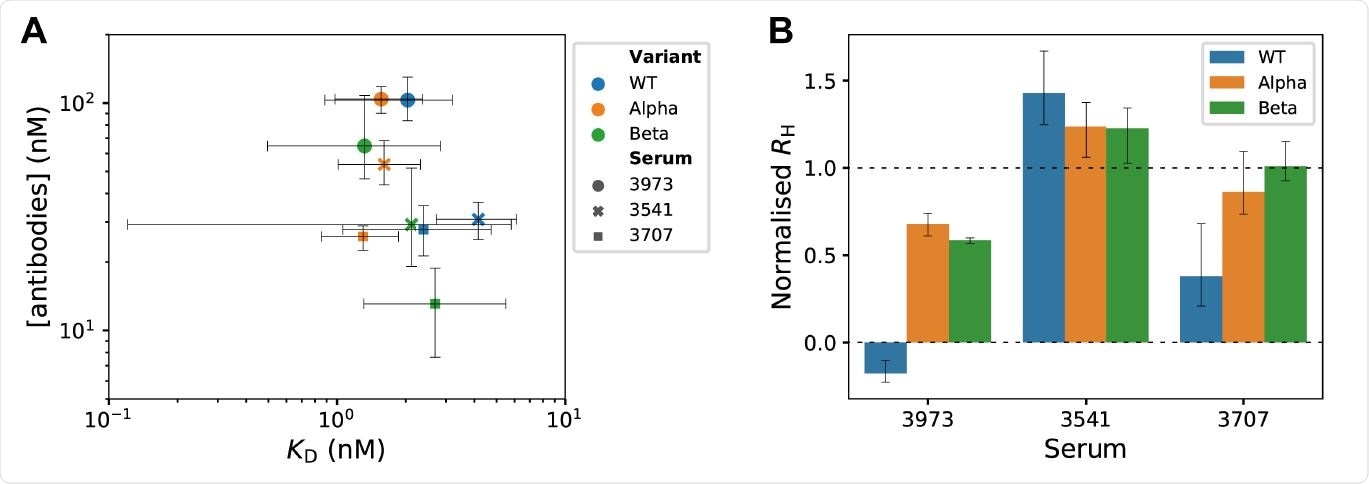
Profilage d’affinité d’anticorps microfluidique et test de compétition de liaison au récepteur en solution dans le sérum de convalescence SARS-CoV-2. (A) La liaison à l’équilibre a été mesurée par dimensionnement diffusionnel microfluidique pour diverses concentrations de variants RBD marqués par fluorescence et de dilutions de sérums convalescents. Les valeurs KD et les concentrations d’anticorps ont été déterminées à partir de modes de distributions de probabilité postérieures obtenues par inférence bayésienne18,19. Les barres d’erreur sont des intervalles crédibles à 95 %. (B) Le test de compétition de liaison au récepteur en solution identifie les anticorps polyclonaux qui déplacent le pic S1 du récepteur ACE2. À Rh normalisé = 0, tout S1 a été déplacé de l’ACE2, et le Rh mesuré est le même que pour l’ACE2 libre. À Rh normalisé = 1, S1 n’a pas été déplacé de ACE2 et le Rh mesuré est le même que pour le complexe ACE2/S1. Les barres d’erreur sont des écarts types obtenus à partir de mesures en triple.
Diverses façons d’échapper à la réponse immunitaire
Les résultats montrent que les anticorps anti-RBD de type sauvage sont plutôt efficaces contre le RBD de type sauvage ; cependant, l’efficacité est beaucoup plus faible pour les variantes alpha et bêta RBD, car elles suivent des approches différentes pour échapper à la réponse immunitaire.
Plus précisément, pour RBD-alpha, l’échappement d’anticorps était principalement dû à une affinité de liaison accrue au récepteur ACE2. En revanche, RBD-beta semble arrêter la liaison des anticorps en modifiant les épitopes clés à la surface de la protéine.
En conséquence, les deux variantes montrent une efficacité accrue dans la liaison à l’ACE2 à la surface des cellules hôtes, augmentant, à son tour, la perspective d’une entrée réussie dans les cellules. Mais, étonnamment, la concentration d’anticorps se liant au RBD-bêta était en fait de moitié par rapport au RBD-alpha et au RBD de type sauvage.
« Nos données suggèrent donc qu’un facteur contribuant à la transmissibilité plus élevée et à l’évasion des anticorps du SRAS-CoV-2 alpha et bêta est une fraction plus importante de virus qui peuvent former un complexe avec ACE2 », déclarent les auteurs de l’étude. « Cependant, les deux variantes utilisent des mécanismes différents pour atteindre cet objectif », ajoutent-ils.
Améliorer notre arsenal thérapeutique
Cette étude a montré que le SARS-CoV-2 alpha RBD peut se lier à l’ACE2 avec une plus grande affinité, ce qui signifie que le déplacement du récepteur par les anticorps neutralisants est beaucoup plus lourd ; cependant, RBD-bêta est moins accessible aux anticorps en raison des changements d’épitope.
Dans tous les cas, ces nouvelles informations quantitatives sur les mécanismes moléculaires complexes de l’échappement des anticorps utilisés par les variantes préoccupantes du SRAS-CoV-2 sont indispensables pour comprendre comment les nouvelles variantes virales évoluent réellement.
En conséquence, cela ouvre la porte au développement de larges candidats thérapeutiques et vaccins qui seront efficaces contre un large éventail de variantes virales actuelles, et qui peuvent être une approche prometteuse contre tout futur mutant viral.
*Avis important
bioRxiv publie des rapports scientifiques préliminaires qui ne sont pas évalués par des pairs et, par conséquent, ne doivent pas être considérés comme concluants, orienter la pratique clinique/le comportement lié à la santé, ou traités comme des informations établies.