Les comorbidités et divers facteurs de risque comme l’âge, l’obésité, les maladies respiratoires chroniques et les maladies cardiovasculaires affectent la gravité de la maladie à coronavirus 2019 (COVID-19). De plus, les symptômes neurologiques sont l’un des symptômes courants du COVID-19, ce qui indique que le virus peut potentiellement infecter et se répliquer dans le système nerveux central (SNC). Cependant, divers éléments de preuve prouvent que le virus ne présente pas de larges propriétés neuroinvasives.
Des encéphalites et des méningites ont été signalées chez plusieurs patients atteints de COVID-19, et de l’ARN et des protéines viraux ont également été identifiés dans le LCR de patients infectés. Bien que les organoïdes du cerveau humain soient vulnérables à l’infection par le coronavirus 2 du syndrome respiratoire aigu sévère (SRAS-CoV-2), une pénétrance étendue du SNC par le SRAS-CoV-2 n’a pas été démontrée. Les modèles animaux précliniques tels que les modèles murins transgéniques de l’enzyme humaine de conversion de l’angiotensine 2 (hACE2) ont fourni des informations clés sur la pathogenèse du COVID-19.
Sommaire
Infection intranasale par le SARS-CoV-2 de souris transgéniques K18-hACE2 pour étudier l’impact neurologique du SARS-CoV-2
Dans une étude récemment publiée sur le bioRxiv* serveur de préimpression, les chercheurs ont tenté d’élargir encore la portée des études précédentes sur l’examen de l’infection par le SRAS-CoV-2 des cellules résidentes du SNC humain. Ils ont évalué la réponse immunitaire à l’infection par le SRAS-CoV-2 du SNC des souris K18-hACE2 et évalué l’influence de la microglie sur la défense de l’hôte après une infection du SNC par le SRAS-CoV-2.
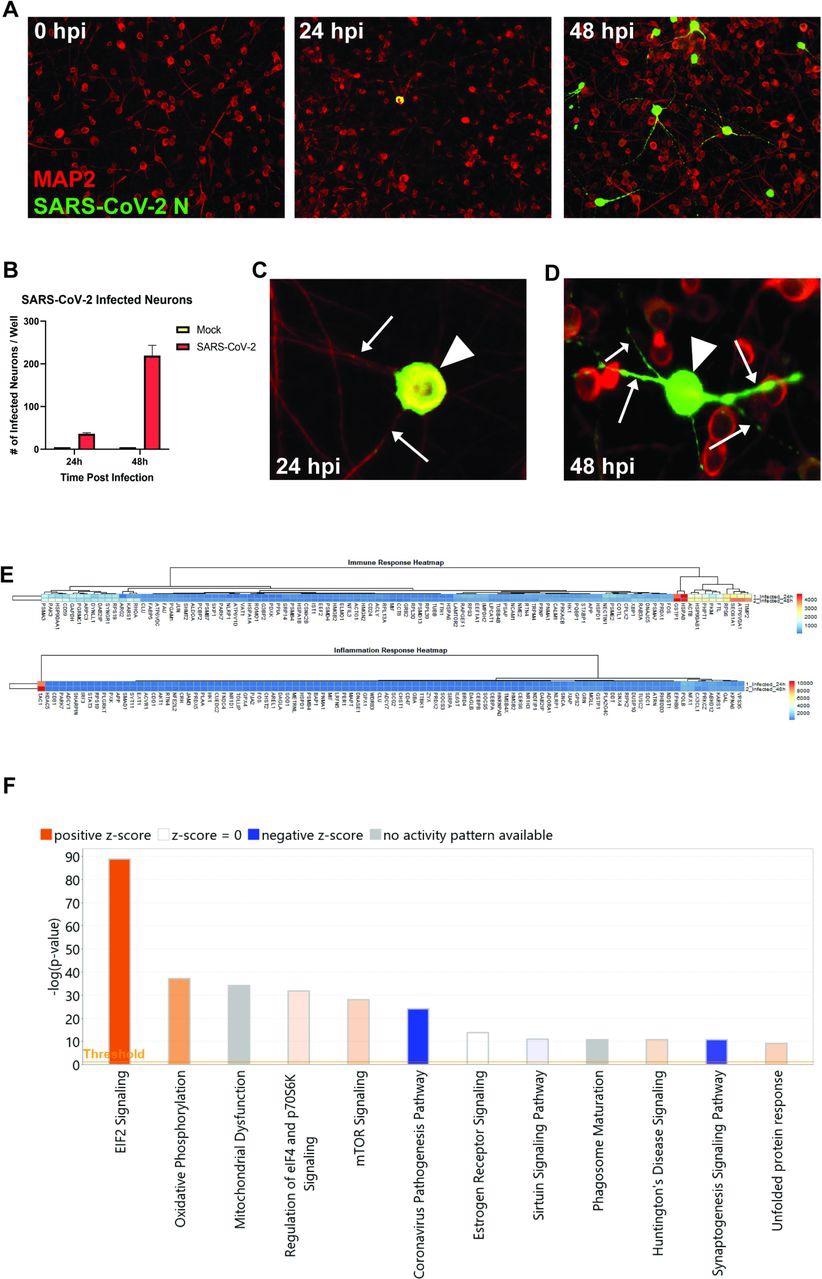
Les neurones humains dérivés d’iPSC ont été inoculés avec le SARS-CoV-2. La coloration des protéines de la nucléocapside a confirmé que le SRAS-CoV-2 était capable d’infecter et de se répliquer dans les neurones. Les observations suggèrent que le virus peut ne pas se propager par fusion avec des cellules voisines puisque la formation de syncytia n’a pas été détectée dans les cultures de neurones. Bien que la voie de pathogenèse du coronavirus ait été surreprésentée, elle a été inhibée en réponse à une infection neuronale par le SRAS-CoV-2.
Infection par le SRAS-CoV-2 de souris K18-hACE2
Des souris K18-hACE2 ont été infectées par voie intranasale avec des unités formant des plaques (PFU) de SARS-CoV-2, et la perte de poids et la mortalité qui en ont résulté ont été enregistrées.
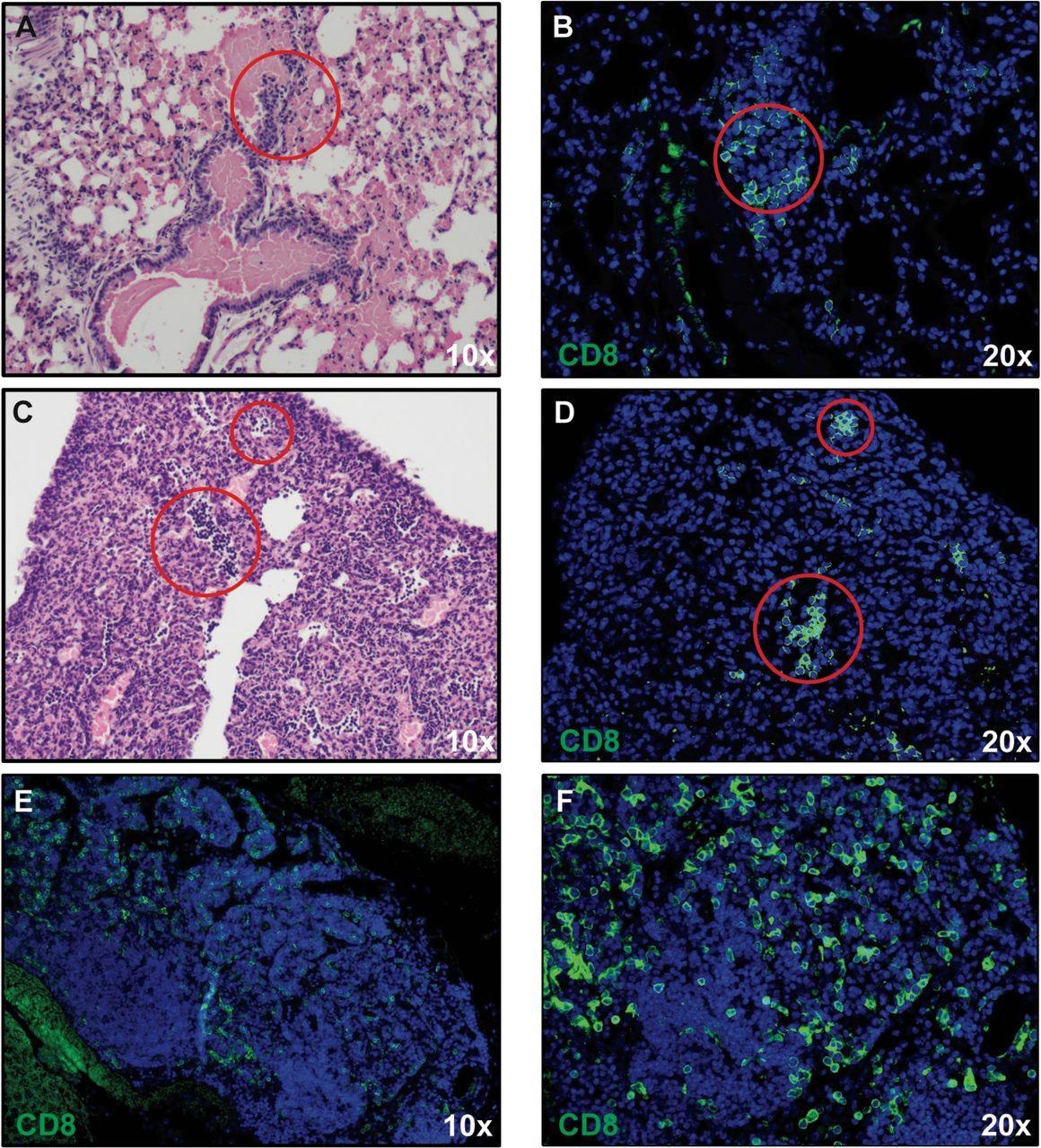
Les résultats ont montré le développement d’une pneumonie interstitielle et d’une infiltration de cellules immunitaires associées à l’ARN viral présent dans les poumons.
L’expression des cytokines pro-inflammatoires (Ifn-λ et Tnf-α)/chimiokines (Cxcl9, Cxcl10, Ccl2, Ccl5 et Ccl19) en réponse à l’infection a augmenté, ce qui est corrélé avec la microgliose et la présence de cellules inflammatoires.
Les chercheurs ont identifié des cellules T CD8+ inflammatoires dans les poumons de souris infectées, qui répondaient vraisemblablement au chimioattracteur des cellules T CXCL10.
De la même manière, des monocytes/macrophages inflammatoires ont probablement été employés en réponse à l’expression de CCL2. La présence de neutrophiles inflammatoires était probablement due à l’augmentation de l’expression des transcrits codant pour CXCR2.
Il a été observé que, chez les souris infectées par le SRAS-CoV-2, l’épuisement de la microglie via l’administration de l’inhibiteur du récepteur du facteur 1 stimulant les colonies PLX5622 n’affectait pas la survie ou la réplication virale. Cependant, l’expression des transcrits de cytokines/chimiokines pro-inflammatoires a été atténuée et une réduction de l’infiltration de monocytes/macrophages a été observée.
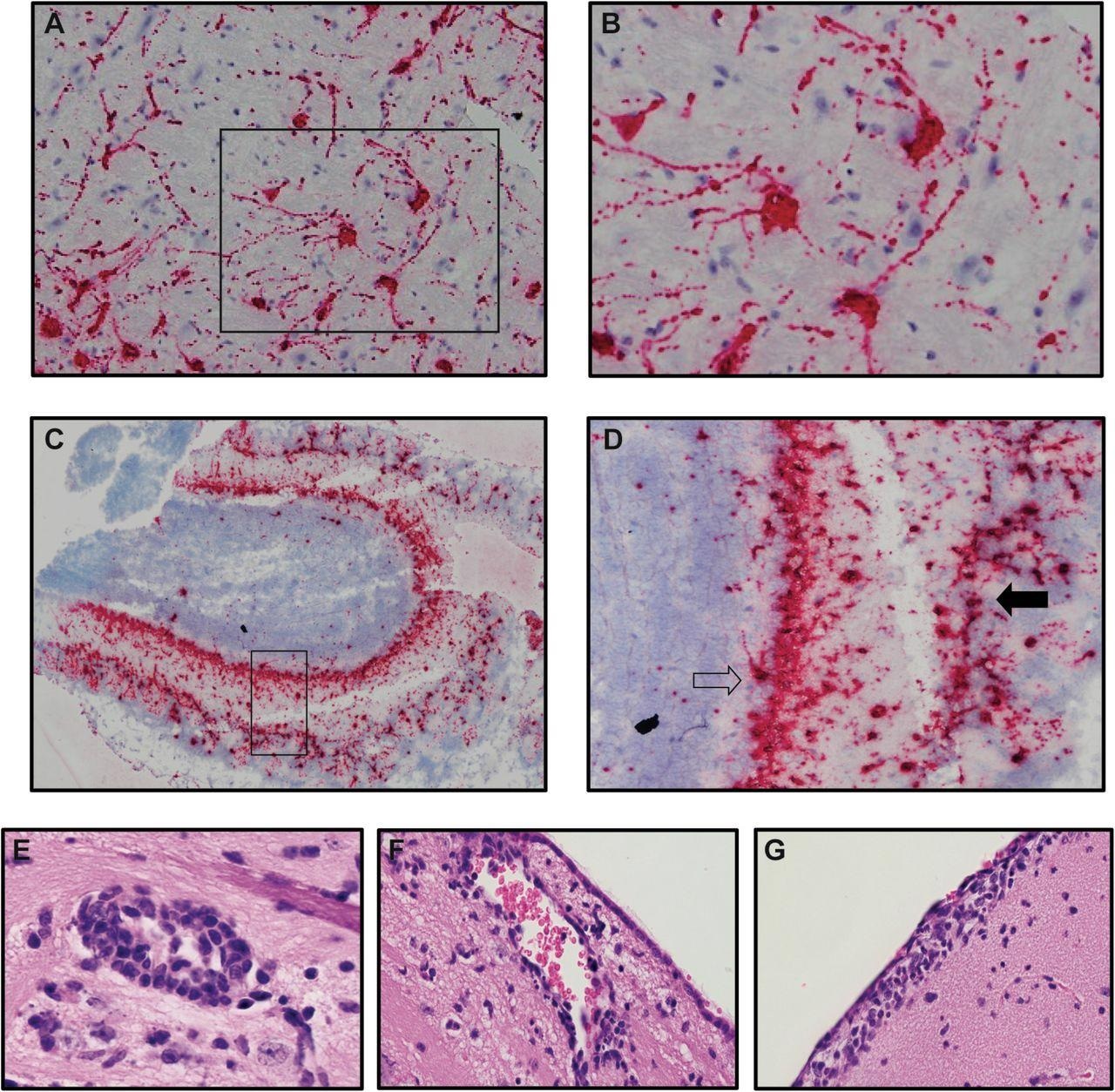
Les résultats de l’étude affirment que la microglie n’a pas joué de rôle dans la réplication du SRAS-CoV-2 dans le modèle K18-hACE2, mais a contribué à une réponse inflammatoire par l’expression de gènes pro-inflammatoires.
Conclusion
La microglie joue un rôle important dans la défense de l’hôte en réponse à une infection virale du SNC. L’ablation de la microglie par l’inhibition du CSF1R entraîne une mortalité accrue chez les souris infectées par le virus du Nil occidental (VNO) et est corrélée à une activation affaiblie des cellules présentatrices d’antigène (APC) et à une réactivation limitée des cellules T spécifiques du virus qui conduit à une clairance virale réduite.
Cette étude a montré que l’épuisement de la microglie chez les souris infectées par le SRAS-CoV-2 n’avait pas d’impact sur la survie ou la réplication virale, mais conduisait à une expression atténuée des cytokines/chimiokines pro-inflammatoires et à une réduction de l’infiltration des monocytes/macrophages.
Les résultats de l’étude s’ajoutent aux rapports précédents indiquant la capacité du SRAS-CoV-2 à infecter les neurones et mettent en évidence l’utilisation potentielle du modèle K18-hACE2 pour étudier les aspects immunologiques et neuropathologiques liés à la maladie neurologique induite par le SRAS-CoV-2.
« Ces résultats soulignent l’importance de travailler avec des modèles animaux dans lesquels l’entrée du SRAS-CoV-2 dans le SNC est plus cohérente avec ce qui a été observé chez les patients COVID-19. »
*Avis important
bioRxiv publie des rapports scientifiques préliminaires qui ne sont pas évalués par des pairs et, par conséquent, ne doivent pas être considérés comme concluants, orienter la pratique clinique/le comportement lié à la santé, ou traités comme des informations établies.