Les symptômes de la maladie à coronavirus 2019 (COVID-19) peuvent persister au-delà de la phase aiguë de l’infection par le coronavirus 2 du syndrome respiratoire aigu sévère (SRAS-CoV-2), généralement environ 28 jours après le diagnostic initial. Les séquelles post-aiguës de la maladie à coronavirus 2019 (PASC), souvent appelées « COVID long », sont souvent utilisées pour décrire la présence de ces symptômes à long terme après la guérison initiale du COVID-19. Le PASC peut entraîner une morbidité importante, malgré la clairance apparente du SRAS-CoV-2 de l’organisme.
Plusieurs mécanismes de développement prolongé du COVID ont été proposés, tels que la persistance du SRAS-CoV-2 ou la dérégulation immunitaire avec des réponses humorales altérées. Cependant, des recherches supplémentaires sont nécessaires pour déterminer les mécanismes exacts responsables de cette condition.
Étude: Impact de l’immunité contre les coronavirus dans les séquelles post-aiguës de COVID-19. Crédit d’image : joshimerbin / Shutterstock.com
Dans une étude récente publiée sur le medRxiv* serveur de prétirage, les chercheurs effectuent un profilage complet des anticorps (Ac) contre le SRAS-CoV-2, plusieurs agents pathogènes endémiques et des antigènes vaccinaux chez les patients atteints de maladies rhumatismales avec ou sans PASC. Ces informations ont été utilisées pour déterminer si le SRAS-CoV-2 ou d’autres réponses humorales ciblées sur les agents pathogènes évoluent uniquement dans le long COVID.
Sommaire
À propos de l’étude
Dans la présente étude, les chercheurs ont exploré les altérations de la réponse immunitaire humorale au SRAS-CoV-2, aux CoV courants, aux herpèsvirus et à plusieurs antigènes vaccinaux pour déterminer si les Abs ciblés sur les agents pathogènes pourraient fournir des informations pertinentes sur la pathogenèse du long COVID. De plus, ils se sont concentrés sur un seul endotype long de COVID, dans lequel ils ont appliqué la sérologie systémique aux patients atteints de maladies rhumatismales qui ont développé une infection légère à modérée par le SRAS-CoV-2, dont 50 % ont développé un long COVID.
À partir du 1er mars 2020, tous les smaladie rhumatismale auto-immune systémique (SARD) les participants avec réaction en chaîne par polymérase (PCR) ou COVID-19 confirmé par l’antigène ont été identifiés par le système de santé du Massachusetts General Brigham (MGB). De plus, les informations sur les patients ont été complétées par des références rhumatologiques de patients infectés par le SRAS-CoV-2.
L’étude comprenait des personnes qui n’avaient pas besoin d’être hospitalisées pour COVID-19 et excluait les personnes ayant des antécédents de fibromyalgie, de maux de dos mécaniques, d’arthrose, de goutte ou de pseudogoutte sans SARD.
Les titres isotypiques spécifiques à l’antigène et la liaison au récepteur Fc (FcR) ont été mesurés par des dosages Luminex multiplexés. Les scores médians d’intensité de fluorescence (MFI) et les valeurs de l’indice d’avidité ont également été calculés.
La phagocytose des neutrophiles dépendante des Ac (ADNP) et des tests séropositifs ont également été effectués. Pour étudier l’enrichissement d’un endotype long particulier de COVID à cause de l’inflammation, les réponses humorales des patients atteints de SARD récupérés au COVID-19 ont été évaluées.
Les profils d’isotype, de sous-classe et de liaison Fc-R contre la nucléocapside du SRAS-CoV-2 (N), la pointe (S), la sous-unité S 2 (S2) et le domaine de liaison au récepteur S (RBD) ont été évalués parmi les deux groupes de malades rhumatismaux. L’équipe a étudié si les altérations des réponses humorales aux vaccins couramment administrés et aux organismes pathogènes endémiques pouvaient fournir des informations sur les différences humorales chez les patients SARD avec ou sans COVID long.
L’équipe a évalué les titres de liaison de l’isotype Ab et du récepteur Fc-gamma (FcγR) sur plusieurs antigènes, y compris les antigènes de routine intégrés au vaccin tels que la rubéole, le tétanos, les oreillons et la rougeole, les virus de l’herpès, y compris le cytomégalovirus (CMV), le virus de l’herpès simplex 1 (HSV1 ), le virus varicelle-zona (VZV) et le virus Epstein Barr (EBV), ainsi que d’autres CoV utilisant les protéines S, S1 et S2 de OC43, HKU1 et SARS-CoV-1.
Réponses humorales contre d’autres pathogènes endémiques tels que le virus respiratoire syncytial (VRS), Staphylococcus aureus, le virus de la grippe et les organismes pathogènes de contrôle tels qu’Ebola ont été évalués. Une analyse discriminante des moindres carrés partiels (PLS-DA) et une régularisation nette élastique ont été effectuées pour visualiser les différences humorales entre les deux groupes.
Résultats de l’étude
Dans l’analyse, 17 patients COVID longs et SARD et 26 patients COVID non longs ont été profilés, 95% vaccinés contre COVID-19. De plus, 79 % des participants à l’étude étaient des femmes.
La polyarthrite rhumatoïde était la maladie rhumatismale la plus fréquemment signalée, tandis que les inhibiteurs du facteur de nécrose tumorale (TNF) étaient les agents thérapeutiques les plus largement utilisés.
Des titres réduits d’immunoglobuline M (IgM) et d’IgG2 anti-SRAS-CoV-2 S et S2, ainsi que des titres d’anticorps inflammatoires ciblés OC43 et CMV plus élevés, ont été observés chez les patients atteints de COVID depuis longtemps. À l’inverse, les individus COVID non longs étaient plus susceptibles de présenter des titres d’isotype/sous-classe plus significatifs, mais pas des titres de liaison FcγR. Les réponses anti-CMV étaient principalement motivées par des déséquilibres de séroprévalence CMV.
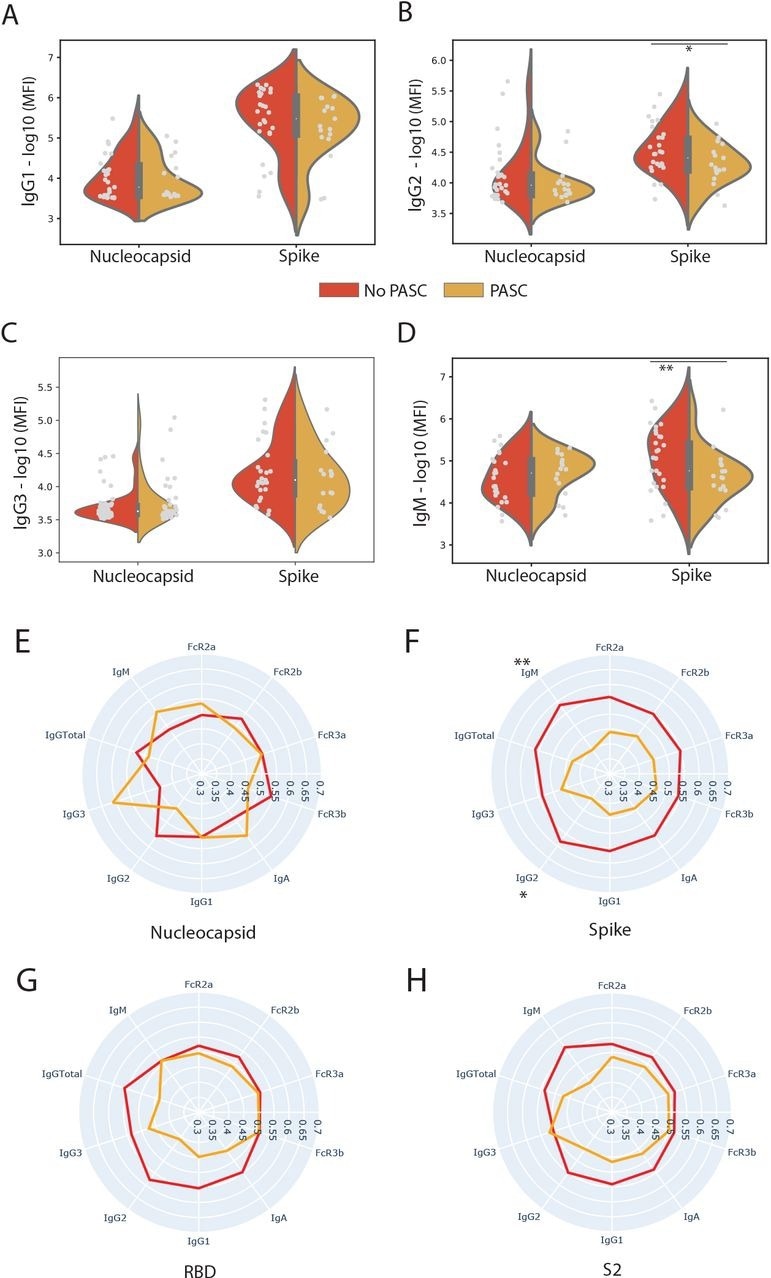
Les réponses dirigées par les pointes du SRAS-CoV-2 sont plus faibles chez les personnes qui en ont fait l’expérience. (A, B, C, D) Les parcelles de violon montrent les titres IgG1, IgG2, IgA1 et IgM contre la nucléocapside du SRAS-CoV-2 (N) et Spike chez les individus qui ont subi le PASC (jaune) et ceux qui ne l’ont pas fait (rouge ). Un test Mann-Whitney U bilatéral a déterminé la signification. (E, F, G, H) Les tracés radar montrent le rang centile moyen des titres d’anticorps et de la liaison au récepteur Fc (FcR) contre la nucléocapside, Spike (domaine Full Spike, RBD et S2) et pour les personnes ayant subi le PASC (Yellow ) et ceux qui ne l’ont pas fait (Rouge). La signification a été déterminée par un test Mann-Whitney U bilatéral. * p = 0,05, p < ** 0,05
Les réponses anti-OC43 étaient principalement induites par des titres d’IgM anti-OC43 de haute avidité. Les réponses OC43 de liaison au FcγR à commutation de classe étaient inversement corrélées à la qualité et à la quantité des réponses humorales anti-SARS-CoV-2.
Notamment, les Abs liant OC43 S FcγR étaient significativement élevés chez les patients COVID longs, tandis que les IgG3 et les titres d’IgM n’étaient pas élevés. Cela indique une expansion des réponses IgG1 hautement inflammatoires au lieu d’une nouvelle évolution de l’Ac OC43 chez les patients COVID de longue date. Pris ensemble, ces résultats suggèrent un rôle potentiel du back-booster commun antérieur du CoV en tant que moteur de la production incomplète d’anticorps anti-SRAS-CoV-2 chez les patients atteints de SARD qui ont développé un long COVID.
Les réponses anti-S2 ont montré une tendance vers des réponses IgG1, IgG2, IgA et IgM plus importantes, ainsi que des FcR opsonophagocytaires spécifiques, y compris FcγR2a et FcγR 2b, chez les patients COVID non longs. De plus, des niveaux élevés d’IgM/IgG3 anti-RSV, de titres de liaison FcγR2a et FcγR2b anti-influenza hémagglutinine (HA), d’IgA anti-SRAS-CoV S1 et d’Ac IgG/IgM antitétaniques ont été sélectivement enrichis en Individus COVID.
En revanche, les titres de liaison anti-OC43 S FcγR3a et FcγR3b et anti-CMV gB FcγR2a/3b/IgM ont été enrichis chez les patients COVID longs. Ainsi, le long COVID semble lié à des réponses humorales de type polyclonal significativement altérées aux vaccins et aux agents pathogènes courants.
conclusion
Dans l’ensemble, les résultats de l’étude mettent en évidence le rôle potentiel de l’empreinte commune antérieure du CoV ou du «péché antigénique originel» dans la maturation incomplète de l’immunité humorale spécifique au SRAS-CoV-2 en tant que marqueur et mécanisme potentiel dans la persistance des longs symptômes de la COVID.
*Avis important
medRxiv publie des rapports scientifiques préliminaires qui ne sont pas évalués par des pairs et, par conséquent, ne doivent pas être considérés comme concluants, guider la pratique clinique/les comportements liés à la santé, ou traités comme des informations établies.