La fibrillation auriculaire (AF) est une forme commune d'arythmie cardiaque, une maladie grave dans laquelle le cœur bat si rapidement que ses chambres supérieures, l'atria, tremblent. Ce rythme cardiaque irrégulier peut augmenter le risque de conditions graves, notamment l'insuffisance cardiaque, la démence et les accidents vasculaires cérébraux.
Mon laboratoire étudie le rôle de l'inflammation dans l'initiation et la persistance de la FA depuis de nombreuses années. Dans cette étude multidisciplinaire, nous avons étudié la fonction de la gasdermin D, un participant clé dans les voies inflammatoires, dans les cellules cardiaques auriculaires et sa contribution potentielle à la FA. «
Dr Na Li, auteur correspondant, professeur de médecine au Baylor College of Medicine
L'œuvre est publiée dans le European Heart Journal.
Des études antérieures ont montré que dans les cellules immunitaires, la gasdermine D est coupée en deux fragments; NT-Gasdermin D, qui peut déclencher la mort cellulaire dans les cellules immunitaires, et le ct-gasdermin D, dont la fonction est inconnue. « Bien que des études antérieures suggèrent que l'activation de la gazdermin D pourrait contribuer à une crise cardiaque en provoquant la mort cellulaire, la fonction précise de la gasdermin D dans les cellules cardiaques reste mal comprise », a déclaré Li.
Les chercheurs ont étudié des sections d'origine humaine pour évaluer les niveaux de gasdermin D et ont trouvé des niveaux accrus de la protéine chez les patients atteints de FA. L'équipe a également travaillé avec un modèle de souris dans lequel ils ont augmenté les niveaux de NT-Gasdermin D uniquement dans les cellules cardiaques auriculaires. « Ces souris avaient une sensibilité accrue à la FA », a déclaré Li.
D'autres études ont montré que le NT-Gasdermin D ne tue pas la plupart des cellules cardiaques mais médie la formation de pores dans la membrane cellulaire. Les pores facilitent la libération de cytokines produites par les cellules cardiaques, des médiateurs immunitaires qui favorisent l'infiltration des cellules immunitaires par rapport aux oreillettes, qui peuvent initier des événements conduisant à un dysfonctionnement auriculaire. Fait intéressant, en même temps, les cellules ont amélioré les mécanismes de réparation membranaire, qui a agi comme une contre-mesure à la formation des pores et a empêché la mort des cellules auriculaires.
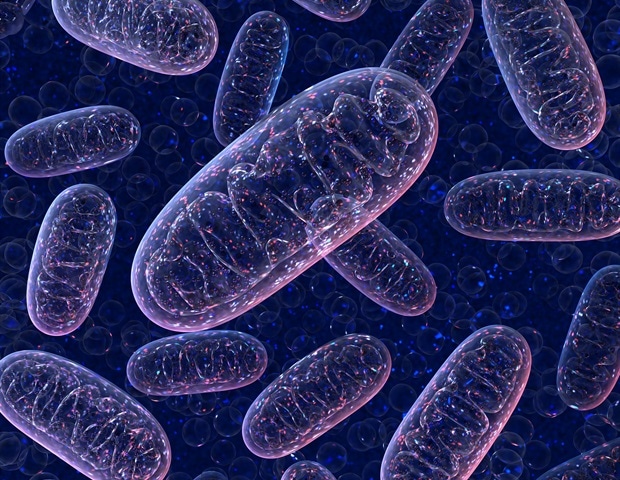
« De plus, le NT-Gasdermin D a ciblé directement les mitochondries, la principale source d'énergie de la cellule, la médiation de la formation des pores et l'augmentation de la libération des espèces mitochondriales d'oxygène réactif (ROS) », a déclaré le premier auteur, le Dr Yue Yuan, associé postdoctoral dans le laboratoire Li. « Alors que ROS se déverse dans les cellules à travers les mitochondries, il déclenche la libération anormale de calcium, qui à son tour favorise des événements qui génèrent des arythmies. »
Soutenant ces résultats, l'équipe a constaté que l'antioxydant spécifique des mitochondries mitotempo, qui récupére les ROS, atténuait les arythmies induites par la NT-Gasdermin D. Un mutant nt-gasdermin d dépourvu de la capacité de former des Pores n'a pas réussi à provoquer une dysfonction mitochondriale ou d'indiquer une arrythmie à l'atriale. Et l'élimination du gène de la gasdermin D a également empêché le développement de la FA spontanée dans le modèle animal.
« Notre étude révèle que le NT-Gasdermin D joue un nouveau rôle dans le développement de la FA à travers des mécanismes multiformes », a déclaré Yuan. « Nos résultats soutiennent que le NT-Gasdermin auTrial contribue aux arythmies cardiaques via un mécanisme unique qui n'implique pas la mort cellulaire mais favorise le dysfonctionnement mitochondrial. »
« Les résultats suggèrent que la thérapie ciblée par mitochondrial, soit en réduisant la production de ROS, soit en inhibant la gasdermin D, peut empêcher le déclenchement de la FA », a déclaré Li. « Cela positionne Gasdermin D comme une cible prometteuse pour une nouvelle option thérapeutique pour la FA. »
Les autres contributeurs à ce travail incluent Pascal Martsch, Xiaohii Chen, Enrique Martinez, Luge Li, Jia Song, Theresa Poppenborg, Florian Bruns, Jong Hwan Kim, Markus Kamler, James F. Martin, Issam Abu-Taha et Dobromir Dobrev. Les auteurs sont affiliés à une ou plusieurs des institutions suivantes: Baylor College of Medicine, University Duisburg-Essen, le Texas Heart Institute et l'Université de Montréal.
Cette étude est soutenue par des subventions des National Institutes of Health (R01HL164838, R01HL136389, R01HL163277, R01HL131517, R01HL089598, R01HL165704, R01HL127717, R01HL169511 et R01HL171574). Un soutien supplémentaire a été fourni par l'American Heart Association (subventions 936111 et 23Post1013888), l'Union européenne (Project Integrative Maestria à grande échelle, n ° 965286), et le Deutsche Forschungsgemeinschaft (Research Training Group 2989, Project 517043330).