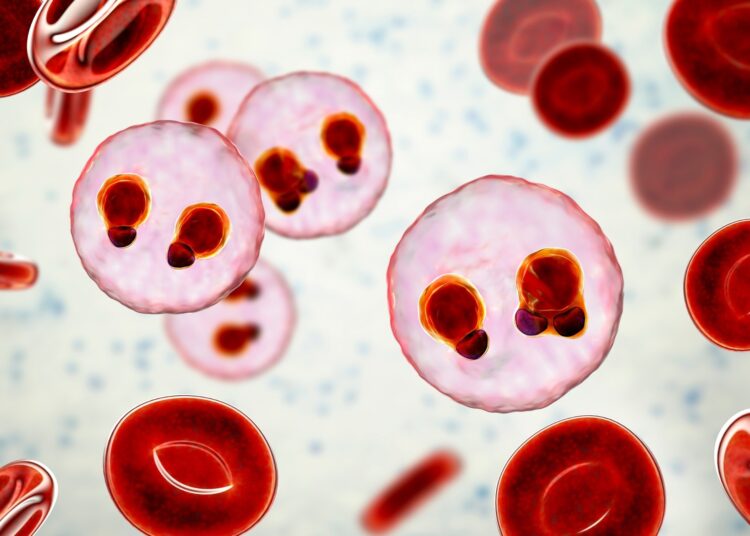
Une étude récente publiée dans la revue Nature Reviews Microbiologie Les vaccins contre le paludisme ont été examinés, ainsi que leurs succès et leurs échecs. Près de la moitié de la population mondiale est exposée au paludisme, les femmes enceintes et les jeunes enfants étant les plus vulnérables. Les femmes et les enfants développent une immunité partielle au fil du temps, ce qui suggère la possibilité d'un vaccin. Le paludisme se manifeste souvent par des symptômes pseudo-grippaux non spécifiques, ce qui entraîne des erreurs de diagnostic et des retards de traitement. Les signes cliniques vont de symptômes légers à des complications graves, et la mortalité reste élevée en l'absence de traitement rapide.
Bilan : Les vaccins contre le paludisme : une nouvelle ère de prévention et de contrôle. Crédit photo : Kateryna Kon / Shutterstock
Le paludisme a tué plus de 600 000 personnes en 2022, un bilan qui ne s'est pas amélioré depuis 2015. Plasmodium espèces responsables du paludisme chez l’homme : P. falciparum, P. vivax, P. ovale, P. malariae, et P. Knowlesi. Parmi ceux-ci, P. falciparum Le paludisme est responsable de la plupart des cas et des décès. Le paludisme peut persister malgré le traitement et l’immunité préexistante. La résistance des parasites aux médicaments et la résistance des moustiques aux insecticides compromettent la lutte contre le paludisme. De plus, les parasites et les moustiques résistants aux interventions existantes se propagent en Afrique et dans d’autres régions. Un rapport a souligné que les facteurs induits par le climat, tels que l’insécurité alimentaire et économique, pourraient déplacer les groupes non immunisés vers les zones d’endémie, augmentant ainsi le risque de transmission du paludisme.

Une illustration du cycle de vie du parasite du paludisme.
Le Rapport mondial sur le paludisme 2023 souligne que l’augmentation de la température, de l’humidité et des précipitations favorise la multiplication des parasites et des vecteurs, accroît l’intensité de la transmission et élargit les zones à risque. Le R21 et le RTS,S sont les premiers vaccins homologués contre le paludisme, ciblant la protéine circumsporozoïte (CSP) des sporozoïtes. Lorsqu’ils sont déployés à grande échelle, ces vaccins peuvent prévenir des décès d’enfants chaque année. Cela donne une impulsion pour améliorer les produits de première génération et poursuivre des objectifs tels que la protection des femmes enceintes et l’éradication du paludisme. Par conséquent, la présente étude a examiné le paysage des vaccins contre le paludisme pour éclairer le développement futur, en soulignant ses succès et ses échecs.
Le vaccin RTS,S est recommandé pour les enfants vivant dans des zones de transmission modérée à élevée afin de réduire le paludisme clinique. Lors des essais de phase III, le vaccin RTS,S a réduit le paludisme clinique d'environ 36 % sur une période de 48 mois à compter de la première dose de vaccin. Le vaccin R21, approuvé par le Ghana et le Nigéria en 2023, a réduit le paludisme clinique au cours des 12 mois suivants d'environ 75 % (administration saisonnière) ou 68 % (administration standard).
Sommaire
Approches du vaccin contre le paludisme en fonction du stade du cycle de vie du parasite
Les vaccins au stade pré-érythrocytaire ciblent les stades hépatiques et les sporozoïtes cliniquement silencieux pour prévenir l'infection. Les parasites intrahépatiques sont ciblés par les lymphocytes T, tandis que les anticorps ciblent les sporozoïtes. Les vaccins au stade sanguin ciblent les protéines d'invasion des mérozoïtes. Parmi les 37 essais de vaccins au stade sanguin entre 2001 et 2015, 32 se sont concentrés sur trois protéines mérozoïtes – l'antigène membranaire apical 1, la protéine de surface mérozoïte 1 (MSP1) et MSP3, qui avaient une efficacité minimale ou nulle dans les études sur le terrain ou les tests de provocation. L'érythrocyte infecté est une cible alternative au stade sanguin ; cependant, la variation de la protéine dominante en surface P. falciparum La famille des protéines membranaires érythrocytaires 1 (PfEMP1) a empêché la mise au point de vaccins à large échelle. Néanmoins, une PfEMP1 distincte, VAR2CSA, pourrait faire exception. Elle est exprimée à la surface des érythrocytes infectés qui se séquestrent dans le placenta, ce qui entraîne des issues défavorables de la grossesse. C'est le principal candidat vaccin contre le paludisme de la grossesse. De plus, les vaccins bloquant la transmission induisent des anticorps contre les antigènes des moustiques ou les parasites au stade sporogonique ou sexuel chez les moustiques.
Limitations, améliorations et optimisations des vaccins
Bien que les vaccins R21 et RTS,S soient des réalisations remarquables, leur protection diminue au fil des ans, ce qui justifie des rappels annuels. En outre, leur efficacité peut varier en fonction de l'intensité de la transmission et du calendrier de vaccination par rapport à la saison de transmission. De plus, les extraits de saponine Quillaja Saponaria sont incorporés dans les adjuvants vaccinaux ; leur approvisionnement n'est pas illimité. De plus, ces vaccins ne sont indiqués que pour les jeunes enfants.
 Quillaja saponaria, l'arbre à écorce de savon, est un arbre à feuilles persistantes de la famille des Quillajacées. Crédit photo : Akif CUBUK / Shutterstock
Quillaja saponaria, l'arbre à écorce de savon, est un arbre à feuilles persistantes de la famille des Quillajacées. Crédit photo : Akif CUBUK / Shutterstock
L'efficacité du R21 dans les essais de phase 3 est supérieure à celle du RTS,S. Bien que les deux vaccins intègrent des P. falciparum Les fragments de CSP (PfCSP), R21 affiche PfCSP sur toutes les sous-unités de capside de l'antigène de surface de l'hépatite B (HBsAg), contrairement à RTS,S, qui s'affiche sur environ 20 % de ces sous-unités. Ainsi, 5 μg de R21 produisent une teneur en PfCSP similaire à celle de 25 μg de RTS,S. Les efforts visant à améliorer le titre et l'activité des vaccins au stade sanguin se sont appuyés sur plusieurs adjuvants, tels que AS02, Alhydrogel et GLA-SE. De plus, les vaccins contre la maladie à coronavirus 2019 (COVID-19) utilisent des nucléotides chimiquement modifiés pour réduire les réponses immunostimulatrices innées. Cette approche a été mise en œuvre pour la protéine riche en glutamate de surface des érythrocytes infectée par P. falciparum (PfGARP), P. vivax protéine de surface des ookinètes 25 (Pvs25) et PfCSP, avec des résultats prometteurs dans les études précliniques. De plus, le dosage fractionné a amélioré l'efficacité du RTS,S contre la provocation par les sporozoïtes. Le dosage fractionné et d'autres régimes sont étudiés pour le R21 Le moment de la vaccination peut être avantageux. Par exemple, l'administration du RTS,S avant la saison de transmission a augmenté l'efficacité. De plus, l'association de la chimioprévention saisonnière du paludisme (SMC) et de la vaccination saisonnière contre le RTS,S a réduit le paludisme clinique de 62,8 % par rapport à la SMC seule.
Répondre aux besoins des communautés endémiques
Les décès fœtaux, néonatals, maternels et infantiles dus au paludisme pendant la grossesse sont très élevés. Les infections traitées pendant la grossesse sont associées à la mort fœtale/néonatale. Par conséquent, des vaccins doivent être développés pour réduire les infections placentaires. L'administration préconceptionnelle du vaccin atténué P. falciparum Le vaccin à sporozoïtes entiers (PfSPZ) s'est avéré efficace contre les infections liées à la grossesse au cours des deux dernières années, ouvrant la voie à des recherches sur les femmes enceintes. P. vivax Le paludisme a causé 18 à 72 % des cas de paludisme dans les zones d'endémie non africaines en 2020. Il génère des hypnozoïtes, c'est-à-dire des parasites dormants, dans le foie, qui récidivent au fil des mois/années, ce qui entrave les efforts d'élimination. De plus, les médicaments qui éliminent les hypnozoïtes provoquent une hémolyse chez les personnes déficientes en glucose-6-phosphate déshydrogénase, ce qui entrave le traitement. P. vivax ont été rares mais efficaces.
Remarques finales
Ensemble, R21 Les vaccins RTS,S et RTS-S réduiront la mortalité infantile après leur déploiement à grande échelle en Afrique. L’association de la vaccination saisonnière et de la chimioprévention a permis de réduire le paludisme d’environ 20 fois par rapport aux taux historiques au Mali et au Burkina Faso, ce qui suggère que des améliorations supplémentaires peuvent être obtenues en matière de santé infantile. En outre, de nouveaux candidats et concepts de vaccins pourraient améliorer l’efficacité de la vaccination et élargir les indications à l’avenir.