Des chercheurs au Royaume-Uni ont mené une étude de cohorte observationnelle sur des patients hospitalisés et ont découvert que le degré de gravité de la maladie à coronavirus aiguë 2019 (COVID-19) prédit la survenue d’une déficience cérébrovasculaire chronique. L’étude suggère en outre que les niveaux de déficience cérébrovasculaire sont associés à une détérioration du bien-être cognitif, mental et physique.
L’anomalie cérébrovasculaire s’est avérée localisée dans les régions latérales frontotemporopariétales du cerveau, et sa signature génétique était responsable de la formation de la composition des types de cellules et du métabolisme.
Une version pré-imprimée du document de recherche est disponible sur le medRxiv* serveur pendant que l’article est soumis à un examen par les pairs.
Étude : L’hospitalisation pour COVID-19 prédit une déficience cérébrovasculaire de longue durée : une étude de cohorte observationnelle prospective. Crédit d’image : SvedOliver/Shutterstock
Sommaire
Fond
Le COVID-19, causé par le coronavirus-2 du syndrome respiratoire aigu sévère (SRAS-CoV-2), a de multiples effets systémiques, y compris des conséquences neurologiques et vasculaires. Il est courant que les patients atteints de COVID-19 souffrent de séquelles neurologiques allant de légers étourdissements, maux de tête et anosmie à une encéphalite sévère, un accident vasculaire cérébral et un délire.
Une mauvaise réactivité cérébrovasculaire, c’est-à-dire la capacité de constriction ou de dilatation des vaisseaux cérébraux du cerveau en réponse à des conditions physiologiques afin de réguler le flux sanguin régional, peut augmenter le risque de neurodégénérescence. De même, les conséquences cérébrovasculaires du COVID-19 peuvent également influencer la santé du cerveau. Bien que cette physiopathologie aiguë soit détectable par neuroimagerie, la persistance des effets à long terme de l’incapacité cérébrovasculaire reste inconnue.
Qu’ont fait les chercheurs ?
Les scientifiques ont évalué la santé cérébrovasculaire de 45 patients hospitalisés, par rapport à la gravité du COVID-19. Les amplitudes de fluctuation à l’état de repos (RSFA), qui est la variabilité du signal dépendant du niveau d’oxygénation du sang (BOLD) au repos, ont été mesurées par imagerie par résonance magnétique fonctionnelle (IRM). RSFA est une méthode robuste, évolutive, sûre et facile à appliquer pour déterminer la réactivité cérébrovasculaire dans les cohortes cliniques. L’étude comportait une comparaison avec 42 témoins appariés selon l’âge et le sexe.
Les données cliniques ont été obtenues à partir des dossiers médicaux électroniques et des évaluations cardiorespiratoires et neurologiques lors des visites de suivi au moins 6 semaines après l’apparition des symptômes.
La gravité de la maladie aiguë a été quantifiée par l’échelle de progression de l’Organisation mondiale de la santé (OMS) COVID-19 et les biomarqueurs sanguins (y compris les biomarqueurs hématologiques, inflammatoires, immunologiques, hépatiques et de coagulation) chez les patients hospitalisés avec COVID-19. L’échelle de progression COVID-19 en 11 points de l’OMS a été utilisée pour évaluer la gravité de la maladie de 0 (non infecté) à 10 (mort).
Des mesures cardiorespiratoires au moins 12 semaines après la sortie de l’hospitalisation initiale avec COVID-19 ont également été recueillies. La qualité de vie, la cognition et la santé mentale ont été évaluées à l’aide d’un ensemble de questionnaires. La prévisibilité de la gravité du COVID-19 sur l’anomalie RSFA a été testée à l’aide d’une approche multivariée.
De plus, le niveau d’anomalies RSFA a été corrélé aux mesures du fonctionnement physique, cognitif et mental (PCM) à l’aide de la régression. En outre, le chevauchement spatial entre les cartes de la charge cérébrovasculaire liée au COVID-19 et une gamme d’expressions métaboliques cérébrales, de neurotransmetteurs et de protéines (y compris l’enzyme de conversion de l’angiotensine-2 [ACE2]; neuropiline-1 [NRP1]; neuropiline-2 [NRP2]) et les paramètres de type cellulaire ont également été évalués.
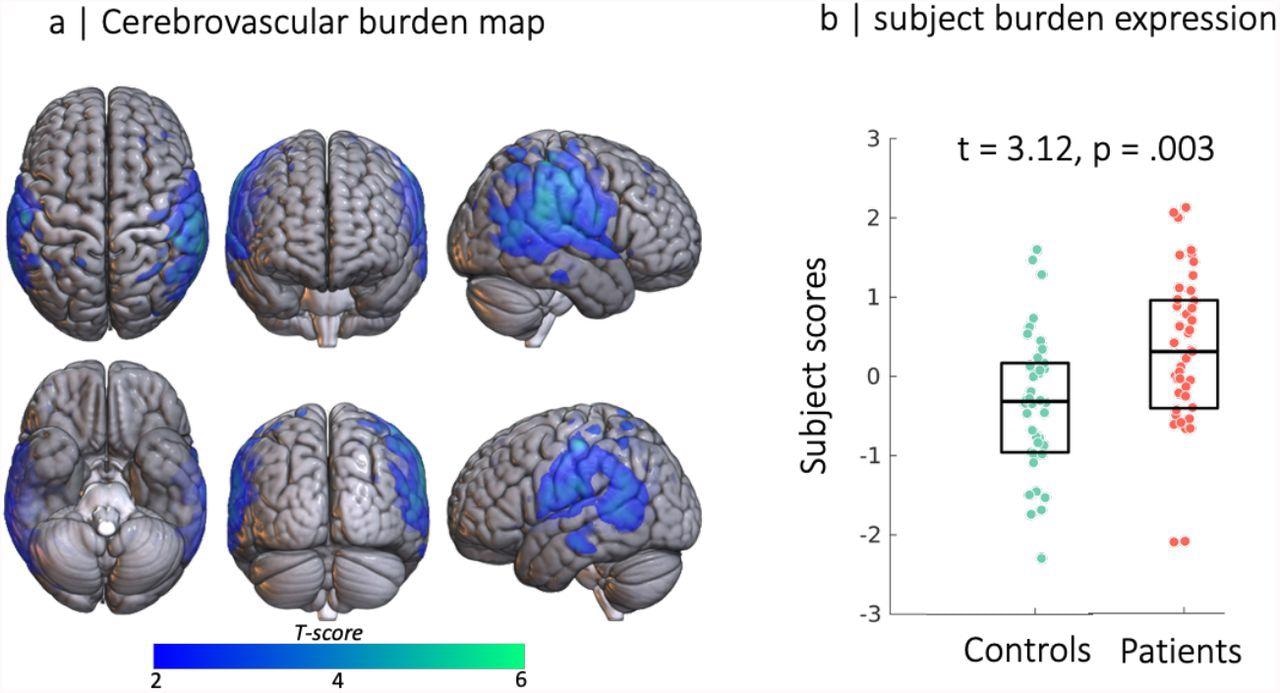
Cérébrovasculométrie basée sur la source pour le composant exprimé de manière différentielle entre les groupes : (à gauche) carte spatiale du composant indépendant reflétant la diminution des valeurs RSFA dans les régions temporo-pariétales. (à droite) Diagramme à barres des scores des sujets pour les patients hospitalisés pour COVID-19 (rouge) et le groupe témoin (vert, chaque cercle représente un individu) indiquant des valeurs de charge plus élevées pour les patients que les témoins, comme indiqué par le test de permutation non apparié à deux échantillons (un test robuste régression a été utilisée pour sous-pondérer les effets des points de données extrêmes)
Qu’ont trouvé les chercheurs ?
L’équipe a observé que l’anomalie cérébrovasculaire, mesurée à l’aide des amplitudes de fluctuation à l’état de repos (RSFA), persistait plusieurs mois après l’hospitalisation pour COVID-19 aigu.
La localisation de ces anomalies s’est avérée être dans les régions latérales, frontales et temporo-pariétales du cerveau, ce qui correspond partiellement au dysfonctionnement cérébrovasculaire rapporté en association avec le vieillissement et la maladie d’Alzheimer préclinique.
Ces effets post-COVID-19 sur la microvascularisation cérébrale étaient liés à la gravité de la maladie aiguë et aux réponses de l’hôte au stade aigu. De plus, ces effets sont également associés à la fonction cognitive post-COVID-19, à la santé mentale et à la qualité de vie six mois après l’hospitalisation.
Un chevauchement a été observé entre la distribution régionale des anomalies vasculaires cérébrales, la distribution spatiale du récepteur vasoréactif 5-HT1b et les régions à forte demande métabolique. Des rapports antérieurs ont impliqué la perte de 5-HT1b dans la perte cognitive progressive, ce qui peut être pertinent pour les conséquences tardives du COVID-19. Cependant, on ne sait toujours pas si la localisation des anomalies RSFA dans les régions riches en récepteurs 5HT-1b est une conséquence de l’hyperactivité de ces récepteurs (avec pour conséquence un faible débit sanguin cérébral), ou de la perte de ces récepteurs (avec vasoparalysie ou inflammation consécutive), ou une manifestation de mésappariement du débit-métabolisme avec un apport inadéquat de substrat et d’oxygène. Ceci est pertinent car les agents thérapeutiques potentiels disponibles modulent à la fois la fonction 5HT-1b et la réponse inflammatoire.
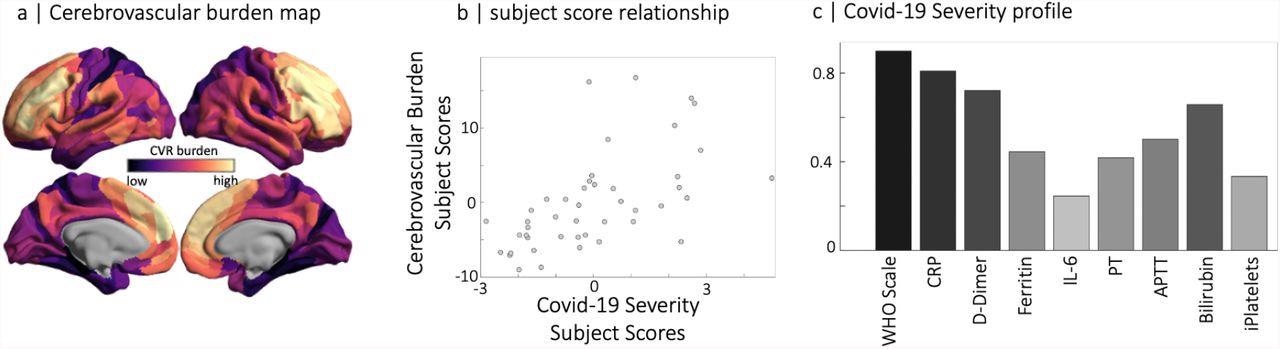
Analyse des moindres carrés partiels des données sur la gravité de la COVID-19 au stade aigu et de la charge cérébrovasculaire (CVB) basée sur la RSFA au stade chronique. (panneau a) Distribution spatiale des valeurs RSFA parcellaires où les couleurs sombres à claires sont utilisées pour la force des corrélations positives et négatives avec le profil de gravité COVID-19 (panneau c). Notez que les régions avec une charge cérébrovasculaire élevée ont de faibles valeurs en RSFA. Le nuage de points dans le panneau du milieu représente la relation entre les scores des sujets de la variable latente RSFA et la variable latente de gravité COVID-19 identifiée par l’analyse des moindres carrés partiels.
Sur la base des résultats, l’équipe établit une corrélation entre les anomalies cérébrovasculaires et la gravité de la maladie via deux interprétations potentielles. L’un pointe vers la possibilité que les altérations de l’intégrité cérébrovasculaire soient les conséquences d’une invasion virale directe, tandis que l’autre pointe vers la conséquence de l’inflammation de l’hôte en réponse à l’invasion virale.
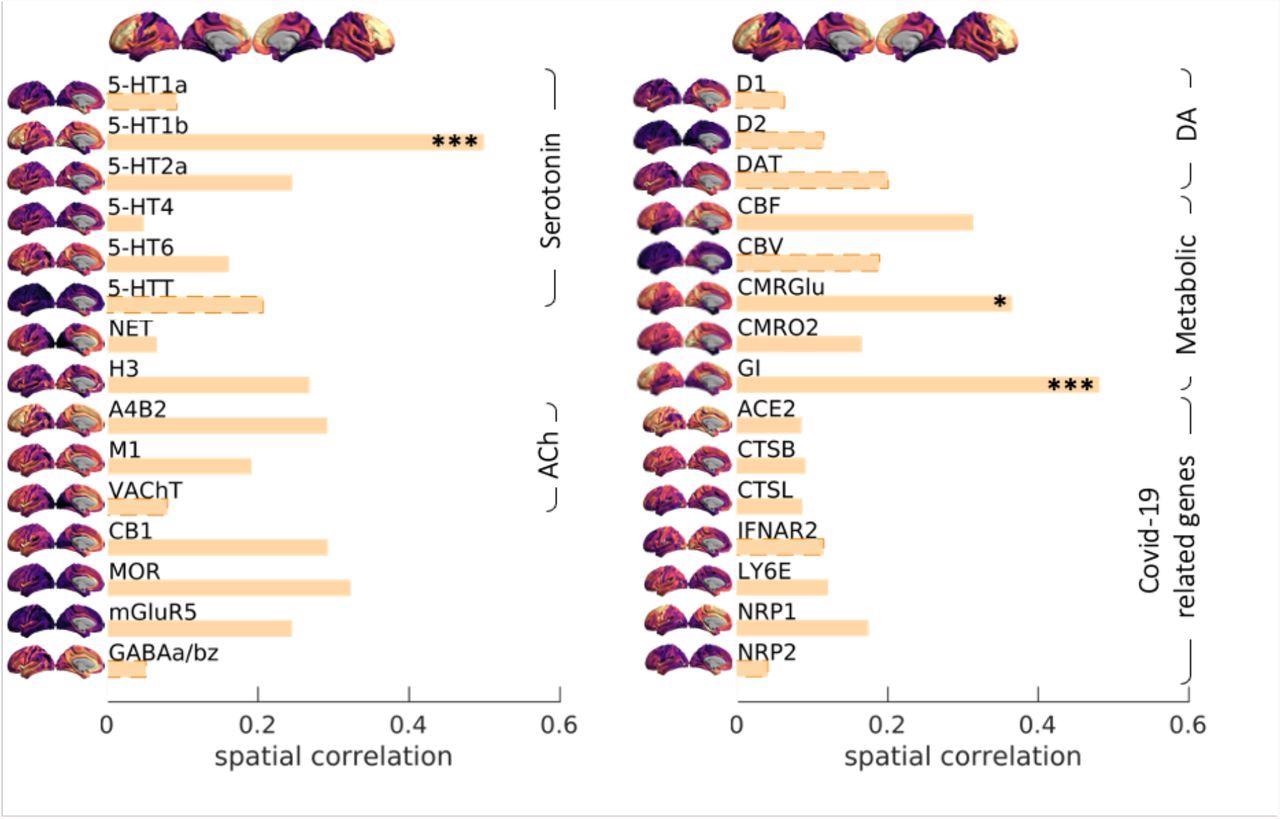
Corrélation spatiale entre la carte de la charge cérébrovasculaire induite par la gravité de Covid19 et les schémas spatiaux associés à une gamme de récepteurs/transporteurs de neurotransmetteurs (Hansen et al., 2021b), gènes sélectifs pertinents pour l’entrée cérébrale du SRAS-CoV-2 (Iadecola et al., 2020) et les paramètres du métabolisme cérébral (Vaishnavi et al., 2010). Les récepteurs et les transporteurs des neurotransmetteurs étaient sélectifs pour la sérotonine (5-HT1a, 5-HT1b, 5-HT2a, 5-HT4, 5-HT6, 5-HTT), la noradrénaline (NET), l’histamine (H3), l’acétylcholine (ACh, A4B2, M1, VAChT), cannabinoïde (CB1), opioïde (MOR), glutamate (mGluR5), GABA (GABAa/bz) et dopamine (D1, D2, DAT). Les cartes métaboliques étaient basées sur le débit sanguin cérébral (CBF), le volume sanguin cérébral (CBV), le taux métabolique cérébral du glucose et de l’oxygène (CMRGlu, CMRO2) et l’index glycémique (IG). Les gènes sélectifs pertinents pour l’entrée cérébrale du SRAS-CoV-2 comprenaient l’enzyme de conversion de l’angiotensine-2, ACE2 ; neuropiline-1, NRP1; neuropiline-2, NRP2, cathepsine-B, CTSB ; cathepsine-L, CTSL, récepteurs de l’interféron de type 2, IFNAR2 ; membre E de la famille 6 de l’antigène lymphocytaire, LY6E. Les cartes spatiales de la 5-HT1b, du CMRGlu et de l’indice glycémique (IG) étaient significativement corrélées avec la carte de la charge cérébrovasculaire induite par la gravité de Covid19 (* p-spin <0,05 (unilatéral), *** p-spin <0,001). Voir le texte pour plus d'informations.
L’équipe n’a pas trouvé d’expression élevée de gènes impliqués dans les réponses cellulaires à l’invasion virale, en particulier ACE2 et Neuropiline-1. La corrélation spatiale de l’anomalie RSFA avec l’expression de tels gènes aurait fourni des preuves à l’appui de l’implication d’une infection virale directe en tant que mécanisme. Mais comme l’équipe n’a pas pu démontrer une telle corrélation, ce résultat défavorable favorise l’interprétation selon laquelle les réponses inflammatoires de l’hôte pourraient entraîner le dysfonctionnement cérébrovasculaire tardif et mériter une enquête plus approfondie.
« L’association d’anomalies microvasculaires avec des résultats tardifs pertinents pour les patients, et le fait qu’ils représentent un biomarqueur facilement accessible, suggèrent à la fois une cible thérapeutique potentielle et/ou un biomarqueur d’effet de traitement dans les études interventionnelles », conclut l’équipe.
*Avis important
medRxiv publie des rapports scientifiques préliminaires qui ne sont pas évalués par des pairs et, par conséquent, ne doivent pas être considérés comme concluants, guider la pratique clinique/les comportements liés à la santé, ou traités comme des informations établies.