Dans une récente étude publiée dans la revue Communication Natureles chercheurs ont cherché à savoir si les vaccins à acide ribonucléique messager (ARNm) contre la maladie à coronavirus 2019 (COVID-19) induisaient des lymphocytes T à mémoire résidente à long terme dans les poumons contre le coronavirus 2 du syndrome respiratoire aigu sévère (SRAS-CoV-2).
Étude : Induction limitée de lymphocytes T à mémoire polyfonctionnelle résidant dans les poumons contre le SRAS-CoV-2 par la vaccination par ARNm par rapport à l’infection. Crédit d’image : piccreative/Shutterstock
Sommaire
Arrière-plan
Alors que les vaccins COVID-19 développés après le début de la pandémie ont réussi à réduire les infections par le SRAS-CoV-2, le niveau de protection de ces vaccins reste incertain. Malgré la baisse de l’efficacité du vaccin au fil du temps et de nouvelles variantes suscitant une immunité humorale, les anticorps neutralisants présentent toujours une protection croisée significative contre le COVID-19.
De plus, l’immunité cellulaire induite par les infections par le SRAS-CoV-2 a été détectée dans le sang périphérique et en tant que lymphocytes T mémoire résidents dans les poumons, le nombre de lymphocytes T mémoire résidents spécifiques au SRAS-CoV-2 étant corrélé au niveau de protection. .
Des recherches récentes indiquent que les vaccins monovalents à ARNm COVID-19, tels que l’ARNm-1273 et le BNT162b2 produits respectivement par Moderna et Pfizer/BioNTech, induisent des niveaux significatifs de CD8+ et CD4+ Les réponses des lymphocytes T dans le sang périphérique et les réponses de l’interféron gamma (IFNγ) contre l’augmentation de la protéine de pointe du SRAS-CoV-2 après des doses de rappel du vaccin à ARNm. Cependant, il reste à déterminer si ces vaccins à ARNm déclenchent des lymphocytes T mémoire spécifiques au SRAS-CoV-2 de longue durée qui résident dans les poumons.
À propos de l’étude
Dans la présente étude, les chercheurs ont comparé des coupes pulmonaires appariées et des échantillons de sang périphérique de quatre cohortes – des individus non vaccinés mais également non infectés, des individus non vaccinés qui étaient en convalescence à long terme du SRAS-CoV-2, des individus qui avaient reçu deux ou trois doses du vaccin à ARNm à long terme mais qui n’avaient pas été infectés, et des individus non infectés qui avaient reçu trois ou quatre doses du vaccin à ARNm à court terme. Les coupes pulmonaires ont été obtenues lorsque les participants ont subi des résections pulmonaires pour des raisons indépendantes, telles que des tumeurs malignes suspectées.
Des pools de peptides constitués de la membrane SARS-CoV-2, de la pointe et des protéines nucléotidiques ont été utilisés pour stimuler les suspensions cellulaires dérivées du tissu pulmonaire et des cellules mononucléaires du sang périphérique (PBMC) obtenues des participants pour examiner les réponses immunitaires cellulaires telles que celles des interleukines (IL)-10, IL-4 et IFNγ. Les niveaux de lymphocytes T spécifiques à la protéine de pointe du SRAS-CoV-2 dans les échantillons de poumon et de sang périphérique ont également été comparés.
Des essais de chimioattraction utilisant des ligands de chimiokine (CCL) 19 et 21 et de la sphingosine-1-phosphate (S1P) ont été utilisés pour attirer la membrane SARS-CoV-2, la pointe et les lymphocytes T spécifiques aux nucléotides dans le tissu pulmonaire pour évaluer la nature du Cellules T résidentes spécifiques de l’antigène dans les poumons. La capacité du vaccin à ARNm à induire des réponses polyfonctionnelles des lymphocytes T spécifiques au pic SARS-CoV-2 dans les poumons et le sang a également été examinée.
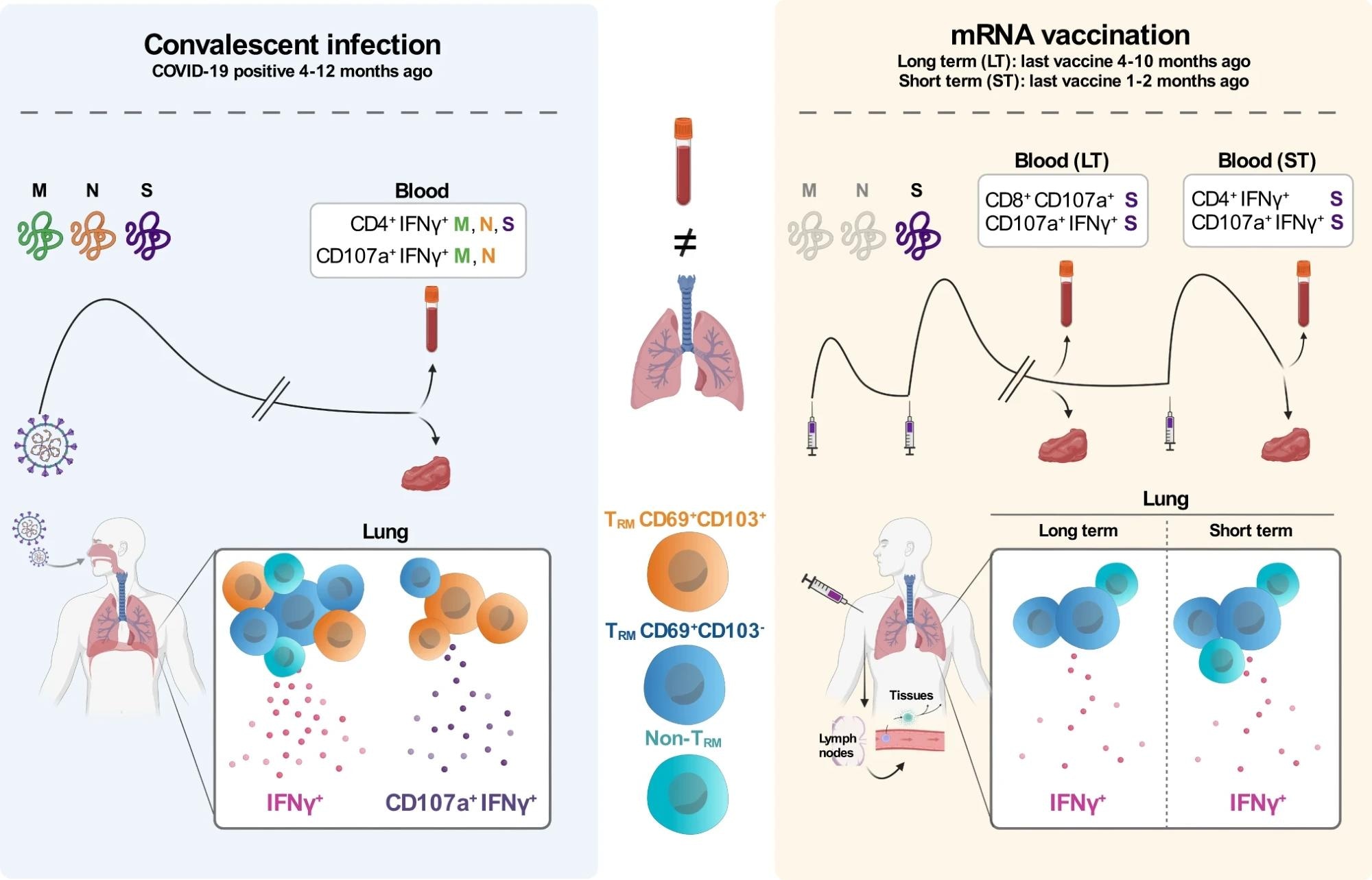 L’objectif de l’étude était d’identifier les réponses des lymphocytes T contre le SRAS-CoV-2 dans des échantillons appariés de sang et de tissu pulmonaire de patients qui se sont rétablis du COVID-19 il y a 4 à 12 mois (infection convalescente, panneau de gauche) et des patients qui n’étaient pas infectés et ARNm vaccinés il y a entre 4 et 10 mois (LT long terme, panneau de droite) ou entre 1 et 2 mois (ST court terme, panneau de droite). À gauche : l’infection par le SRAS-CoV-2 déclenche la réaction du système immunitaire contre plusieurs protéines virales, y compris les protéines M, N et S. Dans le sang des patients convalescents, le CD4+ Les cellules T ont répondu aux peptides M, N et S en produisant de l’IFNγ et des CD4+ et CD8+ Cellules T répondant aux peptides M et N en produisant de l’IFNγ et du CD107a. De plus, dans le poumon de ces patients, nous avons trouvé des lymphocytes T avec principalement du TRM (CD69+CD103+ et CD69+CD103–) phénotypes producteurs d’IFNγ ou d’une combinaison d’IFNγ et de CD107a. À droite : les patients vaccinés par l’ARNm ne sont exposés qu’à l’ARNm codant pour la protéine S du SRAS-CoV-2. Dans le sang des patients vaccinés LT, CD8+ Les cellules T ont répondu aux peptides S en produisant CD107a et CD4+ et CD8+ produisant de l’IFNγ et du CD107a. Dans le sang des patients vaccinés ST, la réponse aux peptides S consistait principalement en CD4+ Cellules T productrices d’IFNγ et de CD4+ et CD8+ produisant de l’IFNγ et du CD107a. Contrairement aux réponses des lymphocytes T dans les poumons des patients infectés en convalescence, les patients vaccinés par ARNm LT et ST ont montré une réponse IFNγ moins importante principalement produite par CD69+CD103– JRM cellules et non-TRM cellules. Dernier, CD69+CD103+ JRM producteurs d’IFNγ et de CD107a étaient pratiquement absents dans les poumons de ces patients vaccinés.
L’objectif de l’étude était d’identifier les réponses des lymphocytes T contre le SRAS-CoV-2 dans des échantillons appariés de sang et de tissu pulmonaire de patients qui se sont rétablis du COVID-19 il y a 4 à 12 mois (infection convalescente, panneau de gauche) et des patients qui n’étaient pas infectés et ARNm vaccinés il y a entre 4 et 10 mois (LT long terme, panneau de droite) ou entre 1 et 2 mois (ST court terme, panneau de droite). À gauche : l’infection par le SRAS-CoV-2 déclenche la réaction du système immunitaire contre plusieurs protéines virales, y compris les protéines M, N et S. Dans le sang des patients convalescents, le CD4+ Les cellules T ont répondu aux peptides M, N et S en produisant de l’IFNγ et des CD4+ et CD8+ Cellules T répondant aux peptides M et N en produisant de l’IFNγ et du CD107a. De plus, dans le poumon de ces patients, nous avons trouvé des lymphocytes T avec principalement du TRM (CD69+CD103+ et CD69+CD103–) phénotypes producteurs d’IFNγ ou d’une combinaison d’IFNγ et de CD107a. À droite : les patients vaccinés par l’ARNm ne sont exposés qu’à l’ARNm codant pour la protéine S du SRAS-CoV-2. Dans le sang des patients vaccinés LT, CD8+ Les cellules T ont répondu aux peptides S en produisant CD107a et CD4+ et CD8+ produisant de l’IFNγ et du CD107a. Dans le sang des patients vaccinés ST, la réponse aux peptides S consistait principalement en CD4+ Cellules T productrices d’IFNγ et de CD4+ et CD8+ produisant de l’IFNγ et du CD107a. Contrairement aux réponses des lymphocytes T dans les poumons des patients infectés en convalescence, les patients vaccinés par ARNm LT et ST ont montré une réponse IFNγ moins importante principalement produite par CD69+CD103– JRM cellules et non-TRM cellules. Dernier, CD69+CD103+ JRM producteurs d’IFNγ et de CD107a étaient pratiquement absents dans les poumons de ces patients vaccinés.
Résultats
Les résultats ont indiqué que si les réponses du CD4 sécrétant de l’IFNγ+ Les lymphocytes T contre la protéine de pointe du SRAS-CoV-2 étaient similaires dans les échantillons pulmonaires obtenus à partir d’individus en convalescence et d’individus immunisés avec le vaccin à ARNm, le phénotype des lymphocytes T à mémoire résidente présenté moins fréquemment dans les réponses pulmonaires des individus vaccinés par rapport à ceux des convalescents. De plus, les cellules T mémoire résidentes polyfonctionnelles présentant l’IFNγ et le marqueur de granulation CD107a étaient presque absentes chez les individus vaccinés à long terme et à court terme.
L’immunité cellulaire induite par l’infection symptomatique par le SRAS-CoV-2 semble également plus forte puisque l’ampleur des réponses immunitaires contre les protéines membranaires et nucléotidiques du SRAS-CoV-2 était supérieure à celle contre la protéine de pointe. Cependant, l’étude a détecté une augmentation des réponses des cellules T sécrétant de l’IFNγ après de récentes doses de rappel du vaccin à ARNm et de l’IFNγ amélioré.+ Cellules T dans les poumons des individus vaccinés à court terme par rapport aux individus vaccinés à long terme.
Les chercheurs pensent que l’incorporation d’autres fragments peptidiques du SRAS-CoV-2, tels que ceux de la protéine nucléocapside, et l’utilisation de l’administration muqueuse dans les futurs vaccins pourraient établir des cellules T à mémoire résidente optimales dans les poumons.
conclusion
Dans l’ensemble, les résultats ont indiqué que les vaccins à ARNm ne provoquent pas de réponses comparables des lymphocytes T à mémoire résidente ou des réponses des lymphocytes T à mémoire résidente polyfonctionnelle contre le SRAS-CoV-2 dans les poumons en tant qu’infections par le SRAS-CoV-2. Les stratégies pour les futurs vaccins pourraient envisager des voies d’administration muqueuses et l’incorporation d’autres protéines du SRAS-CoV-2 pour assurer des réponses plus efficaces des lymphocytes T mémoire.







_a3f42f540aed455c9738e0aa4b52aac3-620x480-e1603380534356.jpg)








