Dans une récente étude publiée sur bioRxiv* serveur de préimpression, une équipe de chercheurs a examiné le répertoire des cellules B mémoire d’individus immunisés avec trois doses de vaccin contre la maladie à coronavirus 2019 (COVID-19) à base d’ARNm.
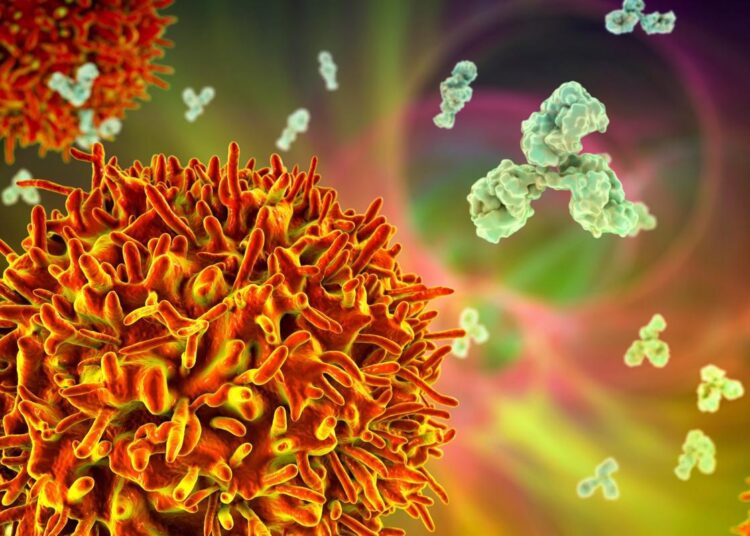
Étude : Augmentation de la puissance et de l’étendue des anticorps neutralisants du SRAS-CoV-2 après une troisième dose de vaccin à ARNm. Crédit d’image : Kateryna Kon/Shutterstock
Les vaccins actuellement utilisés contre le coronavirus 2 (SRAS-CoV-2) contre le syndrome respiratoire aigu sévère à base d’ARNm protègent contre la souche Wuhan-Hu-1 d’origine, mais n’offrent pas une protection complète contre les percées infectieuses (BTI) de toutes les variantes du SRAS-CoV-2 préoccupantes (COV), y compris Omicron. Cependant, des études ont montré que la troisième dose de vaccin à ARNm augmente initialement les anticorps neutralisants anti-Omicron (NAb) circulants avec des titres 10 à 20 fois inférieurs à ceux contre Wuhan-Hu-1, dans de nombreux cas, donc insuffisants pour prévenir les BTI. Par conséquent, des BTI induites par Omicron ont été signalées chez des personnes vaccinées et convalescentes.
Sommaire
À propos de l’étude
Dans la présente étude, les chercheurs ont examiné comment les répertoires de lymphocytes B mémoire chez les personnes ayant reçu la troisième dose de vaccin les protégeaient contre une maladie grave.
Ils ont échantillonné 43 volontaires sans antécédents d’infection par le SRAS-CoV-2 entre le 21 janvier 2021 et le 14 décembre 2021, dont huit et 35 avaient reçu les vaccins Moderna et BNT162b2 à ARNm. Tous les participants étaient dans le groupe d’âge de 23 à 78 ans, et 53 % d’entre eux étaient des hommes et 47 % étaient des femmes.
Les chercheurs ont prélevé des échantillons de sang sur des sujets testés 2,5 semaines après la première dose, 1,3 mois et cinq mois après la deuxième dose de vaccin et un mois après la troisième dose. Les chercheurs ont utilisé des expériences de cytométrie en flux utilisant de la phycoérythrine (PE) et des domaines de liaison aux récepteurs marqués Alexa Fluor 647 (AF647) pour évaluer l’effet de la troisième dose de vaccin sur le compartiment des cellules B mémoire des 43 participants à l’étude.
Résultats de l’étude
Dans des conditions physiologiques normales, les cellules B mémoire ne produisent pas de NAbs. Lorsqu’elles sont mises à l’épreuve avec un antigène comme dans un BTI ou une vaccination, ces cellules subissent une expansion clonale et produisent des plasmocytes sécrétant des anticorps, des mémoires et des cellules B du centre germinal.
Les auteurs ont noté qu’après l’administration de la troisième dose de vaccin aux participants à l’étude, il y avait une augmentation des cellules B mémoire exprimant l’immunoglobuline G (IgG) et les niveaux de CD71 réduits, ce qui suggère que les cellules B mémoire dérivées du centre germinatif dominaient ce compartiment. .
En outre, les clones expansés de lymphocytes B mémoire représentaient respectivement 33 % et 47 % du répertoire cinq mois après la deuxième et un mois après la troisième dose. L’augmentation relative de la clonalité était en partie due à une expansion moyenne de 3,1 fois des cellules B mémoire spécifiques anti-RBD persistantes. Les clones persistants n’ont montré qu’un nombre modéré de divisions cellulaires supplémentaires et n’ont accumulé en moyenne que deux hypermutations somatiques supplémentaires, ce qui rend peu probable que l’expansion clonale supplémentaire nécessite une résidence supplémentaire au centre germinal.
Après la troisième dose de vaccin, il y a eu une augmentation de 1,7 fois (statistiquement insignifiante) du nombre de nouveaux clones uniques de cellules B mémoire. Ces cellules étaient plus mutées que celles présentes cinq mois après la deuxième dose de vaccin, de même que les anticorps représentés une seule fois (singulets). Dans les deux cas, le nombre de mutations somatiques était significativement plus élevé cinq mois après la deuxième dose, indiquant une évolution persistante des lymphocytes B et une division cellulaire.
De plus, après avoir reçu la troisième dose, tous les sujets présentaient des clones expansés de lymphocytes B mémoire et une surreprésentation des gènes variables (VH) 3-30, VH3-53 et VH4-31, indiquant ainsi le biais dans la chaîne lourde des immunoglobulines. La représentation des gènes du gène (IGVH) dans les cellules mémoire est courante chez la plupart des individus.
Les auteurs ont examiné 18 paires d’anticorps appariés de cinq individus échantillonnés cinq mois après avoir reçu la deuxième dose et un mois après avoir reçu la troisième dose pour examiner si ces NAb présentaient une largeur accrue. Comme prévu, la plupart des paires d’anticorps isolées avant et après la troisième dose de vaccin ont montré une neutralisation exceptionnellement large. Alors que 15 des 18 paires d’anticorps ont neutralisé le pseudovirus Delta, 11 ont neutralisé le pseudovirus Omicron. L’analyse par interférométrie de la biocouche (BLI) a montré que ces paires d’anticorps étaient dominées par les classes d’anticorps 1/2, 2/3 et 3.
conclusion
Pour résumer, l’immunisation avec la troisième dose d’un vaccin COVID-19 à base d’ARNm est associée à l’expansion et à l’évolution du compartiment des cellules B mémoire. De plus, ces lymphocytes B produisent des NAb, dont plus de 50 % neutralisent efficacement les pseudovirus Omicron.
Ces observations montrent que les individus ayant reçu trois doses de vaccin ont un répertoire diversifié de lymphocytes B mémoire. Bien que ces lymphocytes B puissent ne pas contribuer aux taux d’anticorps plasmatiques circulants, lorsqu’ils sont confrontés à un antigène sous la forme d’un vaccin ou d’une infection, ils réagissent rapidement et produisent des NAb en 3 à 5 jours capables de neutraliser les variants échappant à l’immunité, tels que Omicron.
Ensemble, les données de l’étude offrent une explication raisonnable de la façon dont la troisième dose d’un vaccin à ARNm non conçu pour protéger contre toutes les variantes du SRAS-CoV-2 pourrait contribuer à la protection renforcée contre le COVID-19 sévère induit par les variantes.
*Avis important
bioRxiv publie des rapports scientifiques préliminaires qui ne sont pas évalués par des pairs et, par conséquent, ne doivent pas être considérés comme concluants, guider la pratique clinique/les comportements liés à la santé, ou traités comme des informations établies.