Après avoir échappé aux chercheurs pendant plus de 30 ans, la protéine VP3 du rotavirus a finalement révélé sa structure et sa fonction uniques à une équipe dirigée par des scientifiques du Baylor College of Medicine.
Les chercheurs ont découvert que VP3 se compose de quatre modules moléculaires qui intègrent de manière unique cinq activités enzymatiques qui sont nécessaires pour coiffer l'ARN messager (ARNm), un processus essentiel pour la synthèse des protéines virales et pour échapper à la réponse immunitaire de l'hôte.
Les chercheurs rapportent dans la revue Avancées scientifiques qu'en plus de deux activités enzymatiques précédemment connues, VP3 présente deux autres activités imprévues, permettant à cette machine de capsulage de remplir une fonction essentielle à la réplication virale.
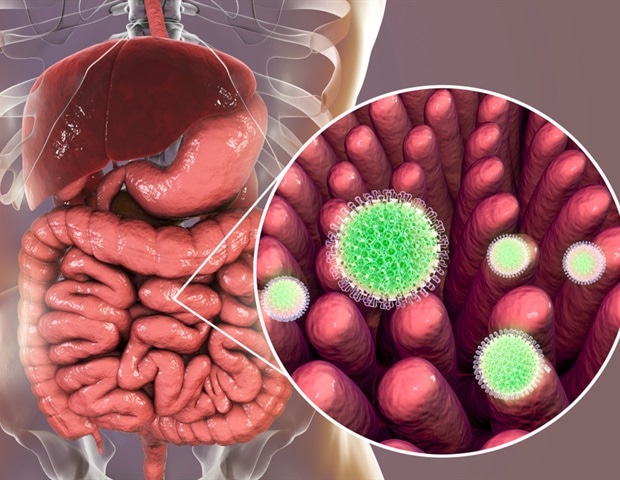
Les résultats ouvrent des opportunités pour concevoir des médicaments antiviraux pour lutter contre l'infection à rotavirus, la cause la plus courante de diarrhée chez les enfants dans le monde, entraînant environ 200 000 décès par an.
« Les virus ne peuvent pas se répliquer par eux-mêmes. Ils prennent le contrôle des machines des cellules qu'ils infectent pour produire des particules virales », a déclaré le co-auteur correspondant, le Dr BV Venkataram Prasad, professeur et président Alvin Romansky du département de biochimie de Verna et Marrs McLean et Biologie moléculaire et professeur de virologie moléculaire et de microbiologie à Baylor.
L'une des stratégies utilisées par les virus pour détourner les cellules qu'ils envahissent consiste à coiffer ou à préparer l'ARNm viral afin qu'il imite l'ARNm coiffé des cellules hôtes. Le coiffage de l'ARNm est une étape essentielle pour engager la machinerie cellulaire qui synthétise les protéines. Imiter le coiffage cellulaire permet au virus de prendre le contrôle de la machine de l'hôte pour produire des protéines virales.
Plusieurs virus utilisent cette stratégie, mais de manières différentes. Dans le cas du rotavirus, il était connu que la protéine virale VP3 était impliquée dans le coiffage, mais pendant plus de trois décennies, déterminer la structure de VP3 et comprendre comment il effectuait le coiffage des ARNm avait été un défi.
La protéine Rotavirus VP3 est une machine de capsulage unique
En combinant la microscopie cryoélectronique, la cristallographie aux rayons X et les analyses biochimiques, nous avons découvert que VP3 possède toutes les activités enzymatiques nécessaires pour coiffer efficacement l'ARNm du rotavirus. Nous avons également constaté que, contrairement à ce qui a été vu dans de nombreux virus qui ont des protéines individuelles pour chaque activité enzymatique, le rotavirus intègre toutes les activités enzymatiques sous forme de modules dans une seule protéine, VP3, «
Dr Dilip Kumar, premier auteur de l'étude et boursier postdoctoral, laboratoire Prasad
« Ce qui rend le rotavirus différent de la plupart des autres virus, c'est que le coiffage a lieu à l'intérieur des limites étroites de la capside virale, la coquille protéique du virus, qui est à l'intérieur de la cellule. Une fois le coiffage terminé, l'ARNm viral quitte la capside par les canaux et entre le cytoplasme de la cellule où il engage la machinerie de production de protéines pour produire des protéines virales « , a déclaré le co-auteur Dr Mary K. Estes, Chaire dotée de la Fondation Cullen et professeur émérite de virologie moléculaire et de microbiologie à Baylor.
« La résolution de ce puzzle était très excitante », a déclaré Kumar. « Nous avons pu isoler VP3 et ses modules et montrer qu'ils s'auto-assemblent en une molécule stable capable de coiffer au moins deux ARNm simultanément, ce qui rend le processus efficace. »
Les collaborations avec le Dr Zhao Wang, professeur adjoint au Département de biochimie et de biologie moléculaire de Verna et Marrs McLean et codirectrice du CryoEM Core à Baylor, et son collègue postdoctoral, le Dr Xinzhe Yu et le Dr Sue Crawford, professeure adjointe en virologie moléculaire et microbiologie pour les dosages enzymatiques et fonctionnels, et Dr Liya Hu, professeure adjointe au Département de biochimie et de biologie moléculaire de Verna et Marrs McLean, pour la modélisation des données cryo-EM.
Prochaines étapes
Connaître la structure de VP3 et son fonctionnement offre la possibilité de concevoir des médicaments antiviraux pour prévenir ou traiter l'infection à rotavirus. De plus, il permet d'étudier plus avant le rôle de VP3 dans la réplication des rotavirus et comment il interfère avec la réponse immunitaire de l'hôte.
« Pendant près de 30 ans, mon laboratoire et le Dr Estes ont collaboré pour démêler la structure complexe du rotavirus et mieux comprendre comment il fonctionne », a déclaré Prasad. « La détermination de la structure et de la fonction de VP3 est une étape importante qui ouvre de nouvelles portes pour poursuivre notre collaboration. »
La source:
Baylor College of Medicine
Référence de la revue:
Kumar, D., et al. (2020) 2,7 Å structure cryo-EM de la protéine centrale du rotavirus VP3, une machine de capsulage unique avec une activité hélicase. Avancées scientifiques. est ce que je.