Dans une récente étude publiée sur bioRxiv* serveur de préimpression, les chercheurs ont démontré que la faible expression de la protéine humaine EXOSC2 protège de la maladie à coronavirus clinique 2019 (COVID-19). Cet effet protecteur s’est fait via la suppression réduite associée à l’expression d’EXOSC2 de la réplication du coronavirus 2 du syndrome respiratoire aigu sévère (SRAS-CoV-2).
La pandémie de COVID-19 en cours est entrée dans une nouvelle phase lorsque des inquiétudes concernant l’efficacité prolongée des vaccins contre le SRAS-CoV-2 sont apparues. Cette inférence était associée à l’incidence accrue d’infections percées par des variants du SRAS-CoV-2 fortement mutés dans les populations hautement vaccinées et à l’incertitude quant à l’efficacité du vaccin à long terme. Par conséquent, les nouvelles cibles de traitement sont une ressource importante dans la lutte pour minimiser la mortalité et la morbidité liées à la pandémie de COVID-19 induite par le SRAS-CoV-2.
La plupart des stratégies de traitement COVID-19 actuellement utilisées fonctionnent en stimulant les réponses immunitaires de l’hôte, en réduisant la réplication virale ou en diminuant l’hyperinflammation. Cependant, seules quelques approches ont tenté de modifier une protéine hôte interagissant avec le virus. De plus, bien que des études d’association à l’échelle du génome (GWAS) aient découvert des loci à risque, certains loci sont liés à des comorbidités et ne sont pas sélectifs des interactions hôte-virus.
Étude : La faible expression d’EXOSC2 protège contre le COVID-19 clinique et empêche la réplication du SRAS-CoV-2. Crédit d’image : NIAID
Sommaire
À propos de l’étude
Dans l’étude actuelle, les scientifiques ont identifié et confirmé expérimentalement une association entre la réduction de l’expression d’EXOSC2 chez l’homme et la réplication réduite du SRAS-CoV-2. Ils ont effectué un dépistage génétique impartial de 332 gènes précédemment identifiés codant pour des protéines hôtes interagissant avec les protéines du SRAS-CoV-2. Pour cela, l’équipe a utilisé des données sur les locus de traits quantitatifs d’expression dérivés du génotype (GTEx) (eQTL).
L’association entre l’expression réduite d’EXOSC2 et l’inhibition de la réplication du SRAS-CoV-2 a été confirmée à l’aide de cellules Calu-3 génétiquement modifiées de l’EXOSC2. En outre, une analyse du transcriptome a également été effectuée.
Résultats
Les résultats ont montré que l’ensemble des 332 protéines hôtes évaluées, dont EXOSC2, interagissaient directement avec les protéines SARS-CoV-2. Pour 208 des 332 protéines hôtes, des eQTL spécifiques aux poumons ont été découverts à l’aide de GTEx (v7). La combinaison des résultats du COVID-19 GWAS pour les eQTL spécifiques au gène a établi un lien entre une expression EXOSC2 plus élevée et une augmentation de la probabilité de COVID-19 clinique qui a réussi diverses corrections de test. EXOSC2 a interagi avec la protéine non structurale 8 (Nsp8) présente dans la polymérase de l’acide ribonucléique (ARN) SARS-CoV-2.
EXOSC2 était un composant d’exosome d’ARN humain. L’ARN polymérase du SRAS-CoV-2 a interagi avec la plupart des constituants de l’exosome d’ARN humain, selon l’analyse de la protéine pulldown par chromatographie liquide avec spectrométrie de masse en tandem (LC-MS-MS). Les composants de l’exosome d’ARN hôte qui ont interagi avec l’ARN polymérase du SRAS-CoV-2 dans les pulldowns Nsp8 marqués par Strep étaient EXOSC10, EXOSC9, EXOSC8, EXOSC7, EXOSC6, EXOSC5, EXOSC4, EXOSC3, EXOSC2 et EXOSC1. En outre, comme pour EXOSC2, une augmentation de l’expression d’EXOSC9 et d’EXOSC7 était également liée à un risque élevé de COVID-19 clinique.
Des mutations non-sens dans les cellules Calu-3 au sein d’EXOSC2 ont été introduites à l’aide de CRISPR/Cas9 et ont entraîné une réduction de la production de protéines EXOSC2 par les cellules. Cette réaction a entravé la réplication du SRAS-CoV-2 et augmenté les gènes de l’oligoadénylate synthase (OAS), ce qui a entraîné une réponse immunitaire efficace ciblant le SRAS-CoV-2. Cependant, la viabilité des cellules hôtes n’a pas été compromise par une expression réduite d’EXOSC2. Des changements dans l’expression du gène OAS se sont produits en l’absence d’élévation considérable d’autres gènes stimulés par l’interféron (ISG) et autonomes à l’infection par le SRAS-CoV-2.
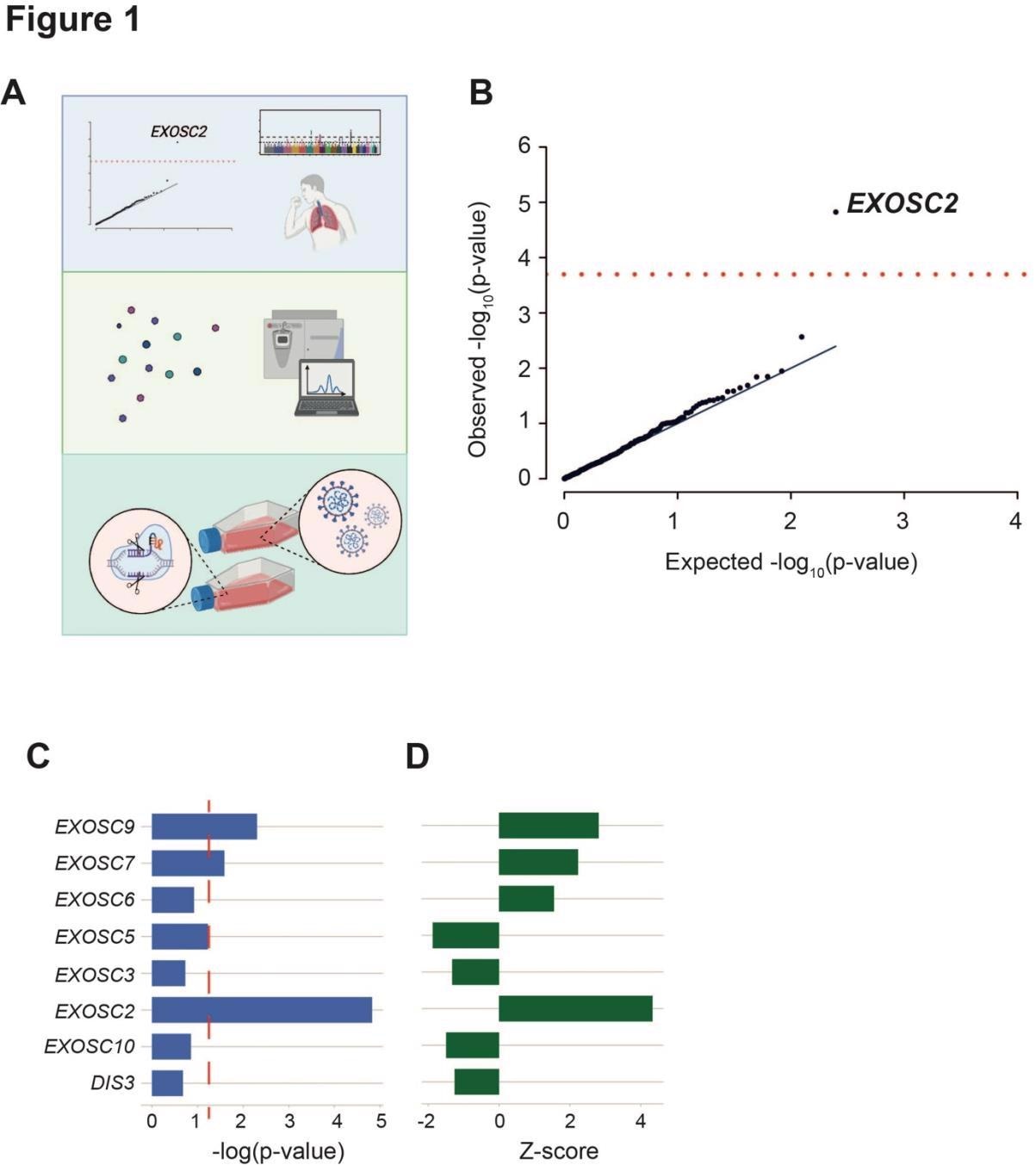
Un dépistage impartial des protéines hôtes identifiées comme des partenaires interagissant avec une confiance élevée des protéines du SRAS-CoV-2 relie les composants de l’exosome d’ARN au risque de COVID-19 clinique. (a) Schéma de la conception de l’étude. Les interactions hôte-virus connues ont été criblées pour l’association de la maladie en combinant des eQTL spécifiques aux poumons avec un GWAS pour les symptômes du COVID-19. L’identification d’une corrélation positive entre l’expression d’EXOSC2 et la gravité accrue de COVID-19 a conduit à une étude plus approfondie des interactions entre la polymérase SARS-CoV-2 et l’exosome d’ARN humain entier par AP-MS. Enfin, l’édition CRISPR d’EXOSC2 dans les cellules pulmonaires humaines et l’infection ultérieure par le SRAS-CoV-2 ont facilité la validation de la relation entre l’expression d’EXOSC2 et la réplication virale et l’interrogation du mécanisme biologique sous-jacent. (b) Les eQTL pulmonaires ont été utilisés pour regrouper les variants génétiques en fonction de leur effet sur l’expression de 332 gènes hôtes codant pour des protéines qui interagissent avec les protéines virales. Seule l’expression d’EXOSC2 était significativement associée au risque clinique de COVID-19 après plusieurs tests de Bonferroni (ligne rouge). ( cd ) Les eQTL pulmonaires ont été utilisés pour regrouper les variantes génétiques en fonction de leur effet sur l’expression de tous les gènes codant pour les composants de l’exosome d’ARN. Les niveaux d’expression d’EXOSC7, EXOSC9 et EXOSC2 étaient significativement liés au COVID-19 clinique et dans chaque cas, une expression plus élevée était associée à un risque d’infection plus élevé. p=0,05 est indiqué par une ligne pointillée rouge.
conclusion
Les résultats de l’étude démontrent qu’une expression réduite d’EXOSC2 a été bien tolérée dans une proportion considérable de la population qui était comparativement immunisée contre le COVID-19 clinique. De plus, aucune toxicité excessive n’a été observée dans les cellules Calu-3 génétiquement modifiées. Cependant, les auteurs n’ont pas identifié le mécanisme lié à l’interaction du SRAS-CoV-2 avec l’exosome d’ARN hôte et les altérations de la réplication virale. Par conséquent, d’autres investigations de biologie structurale sont nécessaires.
Néanmoins, les auteurs ont proposé plusieurs mécanismes potentiels impliqués dans l’interaction de l’exosome d’ARN humain SARS-CoV-2 et les changements dans la réplication du SARS-CoV-2. Les présents résultats suggèrent que la réplication réduite du SRAS-CoV-2 dans les cellules appauvries en EXOSC2 n’était pas significativement liée à une augmentation de l’expression initiale de l’ISG dans ces cellules. En effet, le gène OAS était régulé positivement même en l’absence d’ISG.
Bien que l’étude n’ait pas évalué si les altérations de l’expression de la protéine OAS modulent l’impact d’EXOSC2 sur la réplication du SARS-CoV-2, il pourrait s’agir du mécanisme associant la réplication du SARS-CoV-2 et l’expression d’EXOSC2.
Pour résumer, l’étude a détecté une nouvelle cible thérapeutique, EXOSC2, contre l’infection par le SARS-CoV-2. Il a indiqué que l’inhibition ou l’épuisement ciblé d’EXOSC2 pourrait être un moyen efficace et sûr de protéger les populations à risque contre le COVID-19 cliniquement symptomatique. La recherche actuelle pourrait ajouter de nouvelles perspectives à la thérapie COVID-19 et influencer le développement de nouvelles stratégies de traitement contre le SRAS-CoV-2.
*Avis important
bioRxiv publie des rapports scientifiques préliminaires qui ne sont pas évalués par des pairs et, par conséquent, ne doivent pas être considérés comme concluants, guider la pratique clinique/les comportements liés à la santé, ou traités comme des informations établies.