Les personnes ayant de faibles niveaux d’immunoglobuline et des réponses d’anticorps réduites aux agents pathogènes et aux vaccins sont associées à un déficit immunitaire commun variable (CVID) et à d’autres syndromes de déficit primaire en anticorps (MAP). Généralement, les patients atteints de ces types de troubles immunitaires souffrent d’infections aiguës et récurrentes et courent un risque accru de malignité et d’auto-immunité.
Étude : la stimulation du vaccin par ARNm améliore les réponses des anticorps contre la variante SARS-CoV-2 Omicron chez les patients atteints de syndromes de déficience en anticorps. Crédit d’image : CKA/Shutterstock
Sommaire
Syndromes de déficience en anticorps et COVID-19
CVID n’est pas une maladie particulière. Au lieu de cela, il s’agit d’un ensemble de syndromes d’hypogammaglobulinémie qui surviennent en raison de multiples défauts génétiques. Les chercheurs ont rapporté que le CVID se retrouve chez 1 personne sur 25 000. Il est considéré comme le déficit immunitaire le plus fréquent chez les patients. En règle générale, les personnes atteintes de MAP sont soumises à une thérapie de remplacement d’immunoglobuline intraveineuse ou sous-cutanée qui réduit le risque d’infection.
En réponse à la pandémie de COVID-19, les scientifiques ont conçu des vaccins efficaces contre la protéine de pointe du SRAS-CoV-2.
À ce jour, deux vaccins ont reçu l’approbation complète de la Food and Drug Administration (FDA) des États-Unis, l’ARNm-1273 (Moderna) et le BNT162b2 (Pfizer-BioNTech). L’Ad26.COV2.S (Johnson & Johnson/Janssen) a reçu une autorisation d’utilisation d’urgence (EUA).
Les scientifiques ont déclaré qu’il n’y avait pas beaucoup de preuves disponibles concernant l’efficacité de l’ARNm COVID-19 ou des vaccins à vecteur adénoviral contre l’infection par le SRAS-CoV-2 chez les patients CVID ou PAD. Une étude antérieure a indiqué des taux de séroconversion variables, avec la présence d’anticorps anti-pointe, S1 ou RBD chez 90 % des patients atteints de MAP qui ont reçu le vaccin BNT162b2, ARNm ou ChAdOx1 (Oxford-AstraZeneca). Cette étude a en outre rapporté que de meilleures réponses immunitaires ont été trouvées chez les patients ayant des antécédents d’infection par le SRAS-CoV-2. Cependant, aucune preuve n’a été trouvée concernant la longévité de la protection immunitaire de la vaccination de rappel chez les patients atteints de MAP. En outre, la recherche est rare dans le contexte de la capacité du sérum du patient PAD à neutraliser les variantes du SRAS-CoV-2, en particulier la variante SARS-CoV-2 Omicron actuellement en circulation.
Une nouvelle étude
Une nouvelle étude publiée sur medRxiv* Le serveur de préimpression a évalué l’effet de la vaccination COVID-19 basée sur l’ARNm et de la stratégie de rappel sur les réponses anticorps sériques chez les patients atteints de MAP contre la souche SARS-CoV-2 d’origine et les variantes circulantes. L’étude a révélé que bien que ce groupe de patients présente des réponses humorales altérées, la vaccination a joué un rôle essentiel dans leur protection contre l’infection au COVID-19.
Les chercheurs ont révélé que deux doses de vaccins à ARNm ont généré suffisamment d’anticorps chez la plupart des patients atteints de MAP pour protéger apparemment les individus contre la souche SARS-CoV-2 d’origine ainsi que la variante B.1.617.2. Fait intéressant, les chercheurs ont découvert que les patients atteints de PAD sans antécédents d’infections au COVID-19 présentaient peu ou pas de capacité de neutralisation sérique contre la variante Omicron après deux doses de vaccination. Cependant, lorsque ce groupe a été traité avec un rappel de vaccin à ARNm, un niveau amélioré de réponse anti-Omicron a été observé chez la plupart des individus. De plus, les chercheurs ont découvert que les niveaux d’anticorps neutralisants diminuaient avec le temps.
Les résultats de l’étude sont conformes à un rapport récent du Center for Disease Control and Prevention (CDC) qui suggère un vaccin primaire à trois doses d’ARNm pour les personnes modérément ou sévèrement immunodéprimées. Les scientifiques ont découvert que le niveau de réponse immunitaire chez les patients atteints de PAD avec deux doses de vaccins à ARNm, sans antécédent d’infection au COVID-19, était de moindre ampleur et moins durable que ceux qui se sont remis d’une infection par le SRAS-CoV-2 et ont été vaccinés. Ils ont en outre observé une augmentation des titres neutralisants sériques après la vaccination de rappel par rapport à l’augmentation des titres anti-pointe et anti-RBD. Cette découverte met en évidence l’importance d’effectuer des tests de neutralisation des anticorps en plus des tests de liaison de pointe ou de RBD tout en déterminant la qualité des réponses immunitaires humorales.
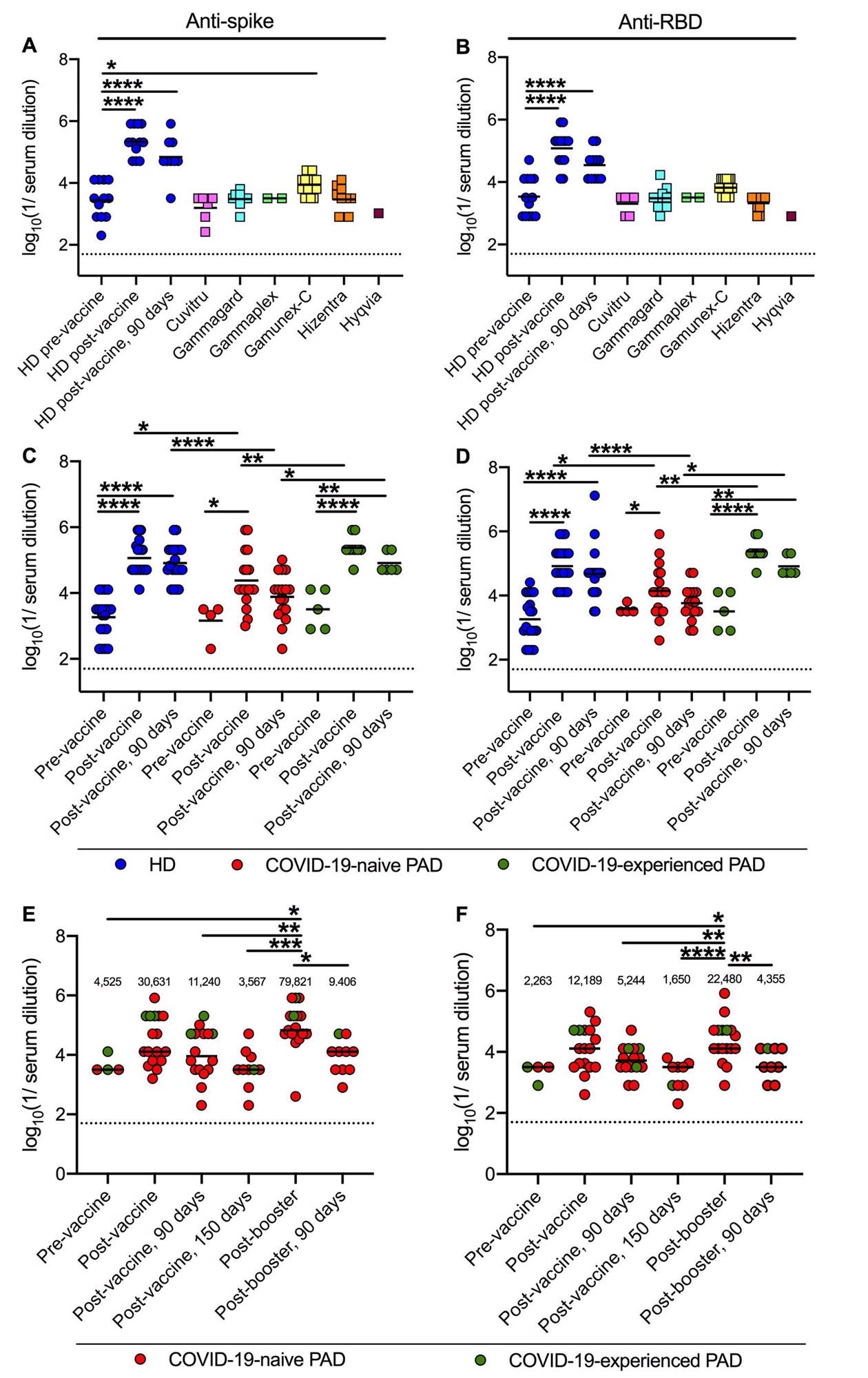
Titres anti-spike et anti-RBD après primovaccination et rappel chez les patients atteints de MAP. Titres des points finaux Anti-Wuhan-1 Spike (A) et RBD (B) dans 48 lots de 6 produits de remplacement d’immunoglobulines différents (carrés) par rapport à 12 HD (cercles bleus) avant, 14 jours et 90 jours après l’achèvement de la série de vaccins BNT162b2 . Titres de point final anti-Wuhan-1 spike (C) et RBD (D) en HD (n = 20 ; cercles bleus), COVID-19-naïf (n = 18 ; cercles rouges) et COVID-19-expérimenté (n = 9 ; cercles verts) patients atteints de MAP avant ou 14 et 90 jours après la fin de la série de vaccinations par ARNm (BNT162b2, n = 19 ou ARNm-1273, n = 8). Titres des points finaux anti-Wuhan-1 Spike (E) et RBD (F) chez les patients naïfs au COVID-19 (n = 14 ; cercles rouges) et les patients atteints de COVID-19 (n = 3 ; cercles verts) avant (n = 4), 14 ou 28 (n = 17), 90 (n = 16) et 150 (n = 10) jours après l’achèvement de l’ARNm primaire (BNT162b2 n = 13, ARNm-1273 n = 2) ou Ad26.COV2. Série de vaccins S (n = 2) et 14 (n = 17) jours et 90 (n = 10) jours après le rappel avec le vaccin à ARNm (BNT162b2 n = 15 ; ou ARNm-1273 n = 2). La ligne noire pointillée représente la limite de détection. Les nombres au-dessus des données représentées graphiquement (EF) représentent le titre moyen géométrique (GMT) pour chaque point dans le temps. ANOVA unidirectionnelle avec post-test de Dunnett ; Les barres indiquent les valeurs moyennes ; Seules les différences significatives sont présentées : *, P < 0,05 ; **, P < 0,01 ; ***, P < 0,001 ; ****, P < 0,0001).
À l’avenir, des recherches supplémentaires sont nécessaires pour évaluer les cellules B dans le sang des patients atteints de MAP après qu’ils aient subi une maturation des anticorps après une infection, une vaccination ou un rappel. Les auteurs ont souligné qu’une des limites de cette étude était l’hétérogénéité de la cohorte de patients atteints de MAP. La cohorte de l’étude comprenait des personnes atteintes de CVID, d’hypogammaglobulinémie ou d’un déficit spécifique en anticorps. Cependant, les scientifiques n’ont observé aucune différence considérable dans les réponses des anticorps aux vaccins à ARNm entre les patients. Il est intéressant de noter que de nombreux patients qui, auparavant, répondaient mal aux antigènes bactériens ou autres protéines (par exemple, l’anatoxine tétanique) ont réagi aux vaccins à ARNm. Bien que la raison précise de cette différence de réaction immunitaire ne soit pas claire, cela pourrait être dû aux propriétés adjuvantes uniques de la nanoparticule lipidique.
Les chercheurs ont signalé qu’aucune réponse d’anticorps n’a été détectée après 90 jours d’immunisation chez les patients atteints de PAD naïfs de COVID avec le vaccin à vecteur adénoviral Ad26.COV2.S. Cette étude indique qu’un vaccin à base d’ARNm peut être plus efficace pour les patients atteints de MAP.
Conclusion
Les scientifiques ont révélé que les titres neutralisants étaient inférieurs au seuil de protection reconnu chez les patients atteints de PAD naïfs au COVID-19. Cependant, la vaccination des patients atteints de MAP avec des vaccins à ARNm ainsi que des rappels est une stratégie efficace pour protéger ce groupe du SRAS-CoV-2 et de ses variantes.
*Avis important
medRxiv publie des rapports scientifiques préliminaires qui ne sont pas évalués par des pairs et, par conséquent, ne doivent pas être considérés comme concluants, guider la pratique clinique/les comportements liés à la santé, ou traités comme des informations établies.