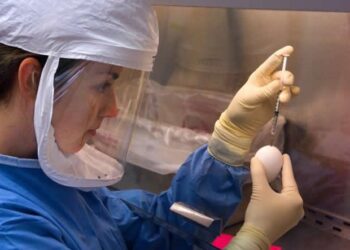
Après avoir examiné plus de 3500 médicaments et petites molécules approuvés par la FDA, des chercheurs de l'Académie chinoise des sciences ont découvert que la ceftazidime, un antibiotique approuvé pour une utilisation dans le traitement de la pneumonie, se lie aux récepteurs que le coronavirus du syndrome respiratoire aigu sévère 2 (SARS-CoV- 2) se lie aux cellules humaines. Ce médicament pourrait potentiellement être utilisé pour prévenir une infection virale. La recherche est publiée sur le bioRxiv* serveur de pré-impression en septembre 2020.
Pour lutter contre la propagation du COVID-19, des chercheurs du monde entier se précipitent pour trouver des stratégies pour empêcher le coronavirus SRAS-CoV-2 d'infecter plus de personnes. Certaines méthodes par lesquelles le virus attaque les cellules humaines sont maintenant connues, et celles-ci ont guidé des approches de traitement.
Le coronavirus contient des protéines, appelées protéines de pointe, qui dépassent de sa surface. Une partie des protéines a des zones appelées domaines de liaison aux récepteurs (RBD) qui peuvent se lier aux récepteurs de l'enzyme de conversion de l'angiotensine 2 (ACE2) trouvée sur les cellules hôtes. Une fois que les RBD se lient aux récepteurs ACE2, le virus peut fusionner avec la membrane de la cellule hôte et infecter la cellule.
Plusieurs stratégies de lutte contre l'infection virale reposent sur la prévention de la liaison du virus aux récepteurs des cellules hôtes. Par exemple, de nombreux anticorps monoclonaux ont été développés qui ciblent la protéine de pointe du virus.
Cependant, ces stratégies ne peuvent pas être déployées immédiatement car elles doivent subir des essais à grande échelle pour l'efficacité et la sécurité chez l'homme, qui ont des délais longs. De plus, le coût des anticorps monoclonaux est très élevé, ce qui peut empêcher son utilisation généralisée.

Criblage de composés à petites molécules qui bloquent spécifiquement l'interaction entre S-RBD et ACE2. a, Diagramme schématique du système AlphaScreen pour détecter l'interaction entre S-RBD et ACE2-ECD. Les billes du donneur et de l'accepteur sont revêtues respectivement de streptavidine et d'anticorps monoclonal anti-His. b, L'interaction entre S-RBD et ACE2-ECD a été surveillée à l'aide du système AlphaScreen 118. c, Comparaison du signal AlphaScreen des protéines S-RBD-His, MAdCAM-1-His et VCAM-1-His en présence ou non d'ACE2-ECD-Biotine dans le système AlphaScreen. d, les bibliothèques utilisées dans le système à haut débit basé sur AlphaScreen, et 75 candidats ont été identifiés à partir de 3581 composés en sélection positive. Le taux d'inhibition a été calculé par la diminution du signal AlphaScreen de chaque composé par rapport à celle du groupe témoin véhicule DMSO. e, diagramme schématique de la sélection négative en utilisant le système AlphaScreen. Le S125 -His biotinylé relie simultanément la bille de donneur enduite de streptavidine et la bille d'accepteur anti-His conjuguée pour générer directement le signal AlphaScreen. f, inhibition relative de 10 composés candidats sur l'interaction S-RBD – ACE2 en utilisant le système AlphaScreen. Le taux d'inhibition relatif a été calculé en soustrayant le taux d'inhibition en sélection négative de celui en sélection positive. g, structure moléculaire de la ceftazidime.
Réutilisation de médicaments connus
Une autre stratégie pour lutter contre le virus consiste à déterminer si des médicaments déjà approuvés pour d'autres maladies peuvent agir contre le SRAS-CoV-2. Étant donné que ces médicaments sont déjà approuvés pour une utilisation chez l'homme, leur utilisation peut être presque immédiate après avoir prouvé qu'ils agissent effectivement dans la prévention du COVID-19.
En utilisant cette idée, les chercheurs ont criblé 3 581 petites molécules de la bibliothèque de médicaments approuvée par la FDA, de la collection Spectrum et de la bibliothèque de composés naturels Targetmol en utilisant une méthode de criblage à haut débit, AlphaScreen.
L'équipe a purifié les RBD et les a attachés à des billes accepteurs et la partie extracellulaire purifiée d'ACE2 à des billes donneuses. Lorsque les RBD se lient à ACE2, les billes accepteurs se rapprochent des billes donneuses. Lors de la lumière brillante d'une longueur d'onde de 680 nm, il y a une émission dans la région 520–620 nm. Un signal plus élevé indique une plus grande affinité. Si les petites molécules criblées empêchent la liaison des billes du donneur et de l'accepteur, ou un signal inférieur, cela indique une inhibition réussie de la liaison des RBD aux récepteurs ACE2.
L'équipe a identifié 75 composés après le premier tour de criblage, montrant au moins 45% d'inhibition. Ils ont affiné leur méthode pour sélectionner 10 composés parmi ces molécules, dont le sulfate de bléomycine, la lévodopa, la noradrénaline, le chlorhydrate de trientine, la ceftazidime, le chiniofon, l'hémateine, la théaflavine, la bléomycine et la myricétine.
La ceftazidime est prometteuse
De ces 10, la ceftazidime était la plus puissante, avec un taux d'inhibition relative d'environ 81%.
La ceftazidime est un type d'antibiotique céphalosporine. C'est un antibiotique généralement utilisé pour traiter la pneumonie bactérienne et est considéré comme sûr, sauf pour les personnes ayant des réactions allergiques aux céphalosporines.
Après des tests supplémentaires sur la ceftazidime, les chercheurs ont découvert qu'elle se lie spécifiquement et fermement aux protéines de pointe RBD, mais pas au domaine extracellulaire ACE2. La ceftazidime a également empêché la liaison des RBD du coronavirus aux cellules épithéliales alvéolaires pulmonaires humaines ou aux cellules pulmonaires, qui expriment également ACE2.
En outre, la ceftazidime a également empêché l'entrée du pseudovirus SARS-CoV-2, une alternative au virus naturel avec une infectivité similaire, dans les cellules exprimant l'ACE2 humaine. La concentration de ceftazidime requise pour une inhibition de 50%, ou la CI50, était d'environ 113 µM, et il n'a montré aucune toxicité mesurable jusqu'à 400 µM.
Dans le traitement de la pneumonie, la concentration sanguine de ceftazidime peut atteindre 300 µM. Les auteurs disent qu'à cette concentration, la ceftazidime a montré une inhibition de 96% de l'infection par le pseudovirus SRAS-CoV-2 in vitro.
Outre la ceftazidime, les chercheurs ont également testé 14 autres céphalosporines, telles que la céphradine et la céfazoline. Cependant, seule la ceftazidime a inhibé la liaison du SARS-CoV-2 à l'ACE2.
Les auteurs pensent que l'action de la ceftazidime est due aux fonctionnalités chimiques du 2-aminothiazole, de l'oxime avec un acide isobutyrique exposé en terminaison et de la pyridine chargée positivement. Ces fragments pourraient interagir avec les RBD de protéine de pointe, empêchant la liaison du virus aux récepteurs ACE2. La forte liaison de la ceftazidime aux RBD suggère une liaison covalente.
En raison de l'inhibition prometteuse de la ceftazidime contre le virus, les auteurs suggèrent que ce médicament devrait être envisagé pour le traitement du COVID-19, d'autant plus qu'il est déjà approuvé, qu'il est sûr et abordable. En outre, des modifications de la structure chimique de la molécule pourraient également être étudiées pour améliorer davantage son action inhibitrice.
*Avis important
bioRxiv publie des rapports scientifiques préliminaires qui ne sont pas évalués par des pairs et, par conséquent, ne doivent pas être considérés comme concluants, orienter la pratique clinique / les comportements liés à la santé ou être traités comme des informations établies.