Le coronavirus 2 du syndrome respiratoire aigu sévère (SRAS-CoV-2) est à l’origine de l’actuelle maladie à coronavirus 2019 (COVID-19). Ce fléau moderne a mis fin aux voyages, aux affaires, à l’éducation et aux loisirs pendant des mois alors que le SRAS-CoV-2 s’est rapidement propagé pour infecter des centaines de millions de personnes dans le monde. Atteindre l’immunité collective est devenu une priorité absolue et qui semblait être à portée de vue une fois que les premiers vaccins ont été développés et se sont avérés sûrs et très efficaces.
Cependant, le coût de la vaccination, les problèmes logistiques et l’émergence de variantes résistantes aux anticorps du SRAS-CoV-2 posent de formidables défis à cet objectif. Une nouvelle étude intéressante publiée sur le preprint medRxiv* introduit la possibilité que le vaccin antipoliomyélitique inactivé, qui fait partie des vaccins universels pour la petite enfance, puisse provoquer des anticorps qui inhibent la synthèse d’acide nucléique du SRAS-CoV-2.
Étude : un vaccin antipoliomyélitique inactivé induit des anticorps qui inhibent la synthèse d’ARN du SRAS-CoV-2 : un essai clinique ouvert pré-post vaccinal. Crédit d’image : Bernard Chantal/Shutterstock.com
Sommaire
Fond
Les quatre premiers vaccins COVID-19 à développer comprennent les vaccins à plate-forme d’acide nucléique de Pfizer/BioNTech et Moderna, ainsi que les vaccins à vecteur d’adénovirus d’AstraZeneca et Johnson & Johnson. Il a été confirmé que tous les vaccins sont capables de réduire le risque d’hospitalisation liée au COVID-19 de 71 % ou plus.
Malgré le déploiement intensif de ces vaccins et de bien d’autres, un peu plus d’un tiers de la population mondiale a été complètement vacciné. En plus des défis susmentionnés, l’hésitation face aux vaccins due aux doutes sur la sécurité des vaccins résultant de la vitesse de développement sans précédent, ainsi que l’utilisation de nouvelles plates-formes, a également affecté le déploiement du vaccin.
La découverte qu’un vaccin existant, couramment utilisé et fiable avait la capacité d’induire une immunité humorale contre le SRAS-CoV-2 serait donc extrêmement gratifiante.
La justification de la recherche d’anticorps anti-SRAS-CoV-2 parmi ceux provoqués par d’autres vaccins provient des premières données collectées au cours de l’effort de développement du vaccin. Ces données étaient basées sur l’hypothèse que les vaccins contre les virus qui ont des similitudes structurelles ou mécaniques avec cet agent pathogène pourraient induire des anticorps contre celui-ci.
Ceci s’applique spécifiquement au vaccin antipoliomyélitique, avec sa protéine non structurale nsp12, également appelée ARN polymérase dépendante de l’acide ribonucléique (ARN) (RdRp). Cette enzyme est essentielle pour tous les virus à ARN, car elle est nécessaire à la synthèse de l’ARN viral et à la réplication virale. Le poliovirus RdRp est étroitement lié à la nucléoprotéine SARS-CoV-2, qui est nécessaire à l’assemblage et à la réplication virales.
À ce titre, les chercheurs ont tenté de développer des médicaments antiviraux spécifiques qui ciblent le RdRp, notamment le remdesivir. Dans le présent article, cette possibilité est explorée plus en détail.
Les anticorps contre le SARS-CoV-2 RdRp se lient au poliovirus RdRp, appelé 3Dpol, sur un ou plusieurs sites. Étant donné que la protéine 3Dpol est incorporée dans le vaccin contre la polio, il est probable que ce vaccin pourrait soutenir efficacement la réponse immunitaire contre le SRAS-CoV-2. Une étude sérologique récente a montré qu’en effet, les anticorps anti-SARS-CoV-2 peuvent être induits par le vaccin antipoliomyélitique.
En d’autres termes, le vaccin antipoliomyélitique inactivé (VPI) suscite une immunité hétérologue telle que les cellules T mémoire peuvent cibler des épitopes partagés entre le poliovirus et le SRAS-CoV-2. Par conséquent, il est possible que l’IPV puisse induire une réponse immunitaire efficace contre le SRAS-CoV-2 et empêcher la réplication virale, indiquant ainsi que le SARS-CoV-2 RdRp est une autre cible pour le développement d’anticorps et de vaccins.
Résultats de l’étude
L’étude actuelle a inclus 300 participants, avec un âge moyen de 51 ans, presque également répartis entre les hommes et les femmes. Aucune de ces personnes n’avait d’antécédents de COVID-19 ou de prise de vaccin COVID-19. Aucun n’avait pris le vaccin antipoliomyélitique au cours des 12 dernières années.
Tous ont reçu une dose de VPI par voie intramusculaire. Au jour 28, leur sang a été testé pour les anticorps anti-poliovirus, y compris les anticorps anti-3Dpol, et les échantillons des participants ont été comparés aux échantillons de base collectés avant la vaccination. Aucun effet secondaire grave n’a été signalé suite à l’immunisation au cours de la première semaine suivant l’injection.
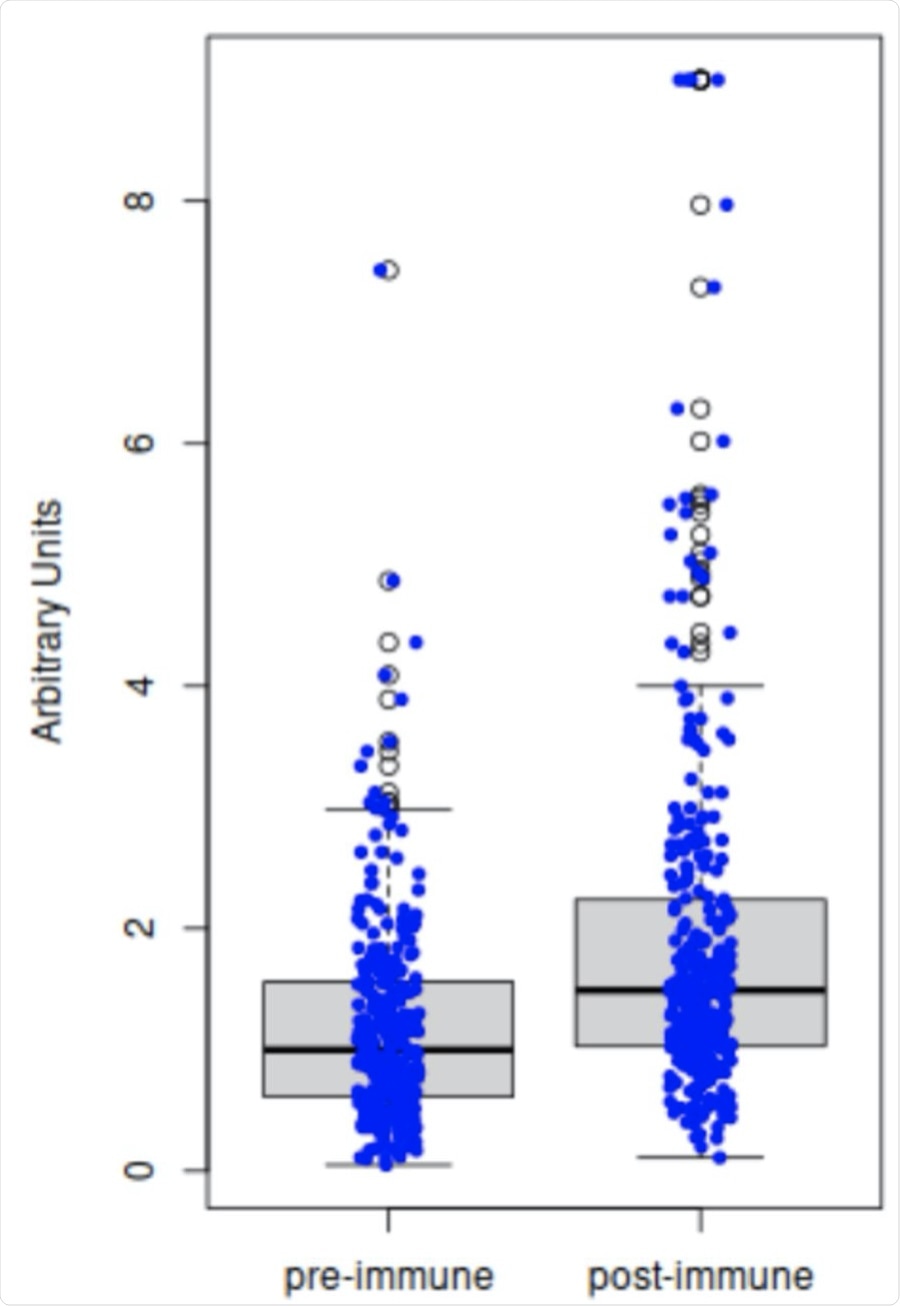 Comparaison des titres d’anticorps pré-inoculation (Jour 1) versus post-inoculation (Jour 28±3). Les résultats de l’ELISA des 298 échantillons de sérum appariés démontrent que l’inoculation avec le vaccin antipoliomyélitique inactivé (VPI) augmente significativement les titres d’anticorps anti-3Dpol (ARN polymérase dépendante de l’ARN, RdRp) chez l’adulte (test t bilatéral, p< 0,001).
Comparaison des titres d’anticorps pré-inoculation (Jour 1) versus post-inoculation (Jour 28±3). Les résultats de l’ELISA des 298 échantillons de sérum appariés démontrent que l’inoculation avec le vaccin antipoliomyélitique inactivé (VPI) augmente significativement les titres d’anticorps anti-3Dpol (ARN polymérase dépendante de l’ARN, RdRp) chez l’adulte (test t bilatéral, p< 0,001).
Cinq participants, soit moins de 2%, ont été testés positifs pour COVID-19 au cours de la période de 28 jours ; cependant, seuls des symptômes bénins tels que fièvre, fatigue et mal de gorge ont été signalés, qui ont tous disparu en 3 jours. À ce jour, aucune hospitalisation ni aucun décès n’a été signalé.
Les anticorps anti-3Dpol ont augmenté par rapport à la ligne de base au cours des 28 jours suivants chez 85% des participants, tandis que 12% ont montré une baisse. Environ 2% étaient inchangés car ils avaient des niveaux d’anticorps élevés au départ.
L’inhibition potentielle de la synthèse d’ARN du SRAS-CoV-2 a également été évaluée en termes d’activité de blocage du sérum contre 3Dpol.
Sur les quelque 300 échantillons post-vaccination, 54 ont été testés au hasard pour l’activité de la polymérase SARS-CoV-2 RdRp. À cette fin, l’activité de la polymérase SARS-CoV-2 RdRp a été régulée à la baisse chez 94% des participants, démontrant ainsi que la synthèse virale de RdRp post-IPV était inhibée. Dans les trois autres cas, les valeurs de RdRp ont été augmentées.
Malgré la variation individuelle, le VPI montre sa capacité à réduire le risque de maladie évolutive dans les cas positifs au COVID-19. Seules trois des 54 personnes étaient susceptibles d’avoir une réplication virale pouvant entraîner une maladie symptomatique.
« Ces résultats montrent que les sérums immunisés contre la poliomyélite sont très susceptibles d’inhiber dans une certaine mesure la synthèse de l’ARN du SRAS-CoV-2, affectant ainsi le processus de réplication virale. «
Implications
Les résultats de la présente étude montrent que l’IPV améliore l’activité anti-3Dpol chez les adultes, en particulier lorsque leurs titres de base sont faibles. Des sérums contenant d’importants anticorps anti-poliovirus ont pu inhiber la synthèse de l’ARN du SRAS-CoV-2.
L’étude démontre également que le VPI peut provoquer des anticorps contre le poliovirus à des titres élevés chez les adultes, tous les participants enregistrant une augmentation des titres d’anticorps au départ, à l’exception de ceux qui avaient déjà des titres préexistants élevés.
Les sérums immuns contenant des anticorps antipoliomyélitiques ont pu bloquer la synthèse d’ARN du SRAS-CoV-2, empêchant ainsi la réplication virale. Plus de 95 % des sérums ont montré une telle activité inhibitrice. Ce résultat est susceptible d’être extrêmement valable dans la pandémie actuelle.
Les résultats de la présente étude corroborent les conclusions d’une étude sérologique antérieure qui montrait que les adultes ayant reçu l’IPV présentaient des titres croissants d’anticorps anti-polio RdRp (3Dpol) qui présentaient une réaction croisée avec la protéine SARS-CoV-2 RdRp. Si cela est confirmé par un essai contrôlé randomisé, cela pourrait signifier un remplacement valable des vaccins vectoriels à ARNm et à adénovirus coûteux par le VPI beaucoup moins coûteux et stable pour la prévention du COVID-19.
La plupart de la population mondiale a déjà été immunisée contre le poliovirus dans le cadre des programmes de vaccination des enfants. Cependant, les très faibles niveaux d’anticorps chez les adultes ne sont probablement pas protecteurs contre le COVID-19, ce qui fait que les résultats de cette étude ne s’appliquent qu’à ceux qui ont reçu une injection de VPI au cours des 28 derniers jours.
Il est important de noter que la cohorte de l’étude représentait un large éventail de troubles médicaux sous-jacents, les seuls critères étant l’absence d’infection active par un agent pathogène et l’absence de grossesse. Cela a été possible grâce au fait que le VPI est un vaccin entièrement approuvé qui est connu pour être extrêmement sûr.
« Cet essai clinique était la première étude de ce genre à évaluer l’IPV dans le contexte de la pandémie de COVID-19. »
D’autres études seront nécessaires pour évaluer le degré de protection dans différents sous-groupes et contre différentes variantes du SRAS-CoV-2. Les études futures pourraient également inclure une population plus importante dans plusieurs centres pour une plus grande généralisation. Cela peut aider à comprendre comment la réponse immunitaire à la VPI se produit dans divers contextes, à travers plusieurs groupes d’âge et origines ethniques.
Une comparaison des sérums d’individus ayant reçu les vaccins COVID-19 et/ou le vaccin IPV serait également utile, ainsi qu’un bras placebo. La durée des titres d’anticorps élevés doit également être évaluée après une, deux ou trois doses d’IPV.
« Ce vaccin facilement disponible pourrait être un moyen de protection inestimable dans les pays à faibles ressources qui n’ont peut-être pas accès à d’autres vaccins COVID-19. Alors que des études plus importantes devraient valider davantage cette affirmation, les données préliminaires de cette étude renforcent les conclusions d’une étude rétrospective antérieure. De plus, cette étude encourage une plus grande considération de l’utilisation du VPI comme agent thérapeutique potentiel qui est plus facilement disponible dans les pays à faibles ressources, ainsi qu’un vaccin bien établi qui peut être considéré comme une option plus sûre et plus largement fiable pour les hésitants à la vaccination. populations. «
*Avis important
medRxiv publie des rapports scientifiques préliminaires qui ne sont pas évalués par des pairs et, par conséquent, ne doivent pas être considérés comme concluants, orienter la pratique clinique/le comportement lié à la santé, ou traités comme des informations établies.