Causée par l’agent du coronavirus 2 du syndrome respiratoire aigu sévère (SRAS-CoV-2), la pandémie de la maladie du coronavirus 2019 (COVID-19) a maintenant atteint plus de 191 pays et infecté plus de 63,98 millions de personnes. Les scientifiques du monde entier se précipitent pour mieux comprendre le virus, comment il se transmet et comment il affecte le corps.
Une équipe de chercheurs de l’Université de Hong Kong a identifié un panel de variantes du SRAS-CoV-2, appelé Del-mut, qui contient une suppression dans la jonction S1 / S2. Après avoir étudié l’une des variantes supprimées dans des modèles animaux, ils ont constaté que Del-mut-1 est atténué dans sa capacité à provoquer des maladies ou des changements pathologiques.

L’émergence du SRAS-CoV-2
L’agent pathogène SRAS-CoV-2 a été détecté pour la première fois dans la ville de Wuhan, en Chine, en décembre 2019. Depuis lors, il s’est propagé rapidement à travers le monde, tuant plus de 1,481 million de personnes.
L’origine exacte du virus reste insaisissable. Pourtant, la présence d’un motif distinct dans la jonction S1 / S2 suggère l’acquisition possible de sites de clivage dans la protéine de pointe qui a favorisé la zoonose ou la transmission interspécifique.
La zoonose survient lorsque des agents pathogènes d’origine animale se dirigent vers les hôtes humains et provoquent une infection. Le virus s’adapte alors au corps humain et commence à se transmettre entre les hôtes humains.
La protéine de pointe du virus – les pointes saillantes qui tapissent son enveloppe – se lie au récepteur de l’enzyme de conversion de l’angiotensine 2 (ACE2) de la cellule humaine, qui agit comme une passerelle cellulaire pour l’entrée virale.
L’analyse génétique du virus a révélé un lien génétique potentiel entre le SRAS-CoV-2 et les coronavirus identifiés chez les chauves-souris du Yunnan, en Chine. Cependant, il n’y a toujours pas de virus ancestral direct ou d’hôte intermédiaire pour la transmission interspécifique du SRAS-CoV-2 aux humains.
Pendant ce temps, les scientifiques suggèrent qu’une transmission interhumaine efficace semble s’être produite dès que l’épidémie de SRAS-CoV-2 a été détectée. La dynamique de l’excrétion virale et la réponse de l’hôte au stade précoce de l’apparition de la maladie montrent que le virus a une capacité de transmission humaine unique.
L’étude
Dans l’étude, publiée dans la revue Microbes émergents et infection, les chercheurs ont trouvé une série de variantes contenant des délétions de 15-30 pb (Del-mut) ou des mutations ponctuelles à la jonction S1 / S2. Ils ont également examiné l’échantillon clinique d’origine où l’isolement a été obtenu, et 26 autres échantillons cliniques positifs pour le SRAS-CoV-2 n’ont pas réussi à détecter ces variantes.
Pour approfondir l’enquête, l’équipe a inoculé le virus à des hamsters et a découvert que l’une des variantes, le Del-mut-1, qui porte une suppression de dix acides aminés, ne provoque pas de perte de poids ou de changements pathologiques plus graves dans les poumons, ce qui est liée à l’infection par le virus de type sauvage.
L’équipe a noté que le motif de clivage unique qui favorise l’infection par le SRAS-CoV-2 chez l’homme pourrait être confronté à une forte pression sélective, car la réplication dans des cellules Vero-E6 permissives conduit à la perte de cette fonction adaptative. Cela confirme l’affirmation selon laquelle la fonction acquise de l’insertion de jonction S1 / S2 n’est nécessaire que pour une réplication non permissive.
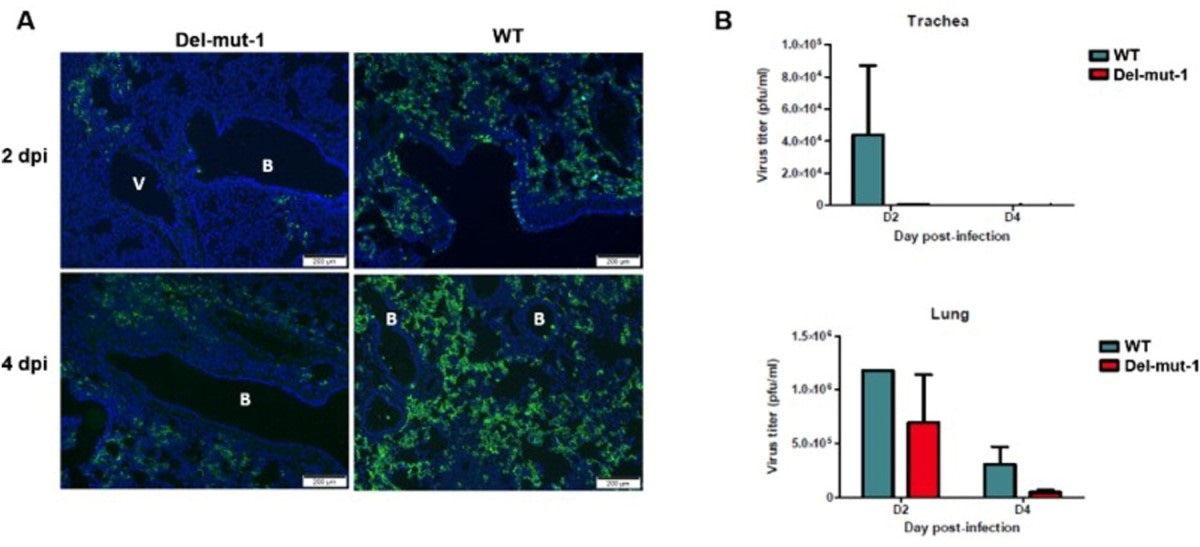
Réplication du virus dans les tissus pulmonaires de hamsters infectés par le virus WT ou Del-mut-1 SARS-CoV-2. (A) Test d’immunofluorescence indirecte avec des anticorps contre la protéine N du virus SARS-CoV-2 (vert). Bleu: coloration DAPI des noyaux cellulaires. B: bronchiole, V: vaisseau sanguin. (B) Titrage du virus par dosage de la plaque des tissus pulmonaires et trachéaux collectés aux jours 2 et 4 après l’infection. Les barres d’erreur représentent la moyenne ± sd (n = 2 par groupe pour chaque point temporel) Barre d’échelle, 200 µm, dpi: jours après l’infection.
Une enquête plus approfondie est nécessaire pour déterminer si la transmissibilité exceptionnelle du SRAS-CoV-2 est liée à la fonction acquise de l’insertion de la jonction S1 / S2. À l’heure actuelle, les coronavirus humains en circulation, comme celui qui cause le rhume, ne contiennent pas de motif principal dans la jonction S1 / S2.
Par conséquent, si le SARS-CoV-2 doit devenir un virus humain complet, l’un des variants de Del-mut pourrait être la forme finale du virus. Étant donné que le variant Del-mut-1 ne provoque pas de maladie grave chez les animaux, sa forme atténuée peut être utilisée pour effectuer des recherches de dépistage de médicaments ou des études fonctionnelles dans des laboratoires où une installation de biosécurité de haut niveau n’est pas disponible.
<< L'un des besoins les plus urgents en réponse au COVID-19 est le développement d'un vaccin efficace pour contenir la pandémie en cours et en préparation pour la prévalence à long terme du virus SRAS-CoV-2. L'innocuité et le potentiel vaccinal du Del- mut variantes devraient également être explorées », a conclu l'équipe dans l'étude.
Jusqu’à présent, dix vaccins candidats en sont à la dernière étape des essais sur l’homme et deux attendent l’approbation de l’organisme de réglementation. Alors que de nouvelles informations sur le virus émergent continuellement, les scientifiques doivent considérer cela comme une base pour développer de nouveaux vaccins efficaces et sûrs pour lutter contre le COVID-19.
La source:
Référence du journal:
- Lau, SY, Wang, P., Mok, BWY, Zhang, A., Chu, H., Lee, A., et al. (2020). Variantes SARS-CoV-2 atténuées avec suppressions à la jonction S1 / S2. Microbes émergents et infection. https: //doi/10.1080/22221751.2020.175670, https://www.tandfonline.com/doi/full/10.1080/22221751.2020.175670



























